
����Ŀ����֪����298KʱK(HF)=3.5��10-4��Ksp(CaF2)=1.8��10-7
��HF(aq)![]() H+(aq)+F-(aq)��H<0
H+(aq)+F-(aq)��H<0
����������֪��Ϣ�ж�����˵����ȷ���ǣ� ��
A. 298Kʱ��������ˮϡ��HF��Һ�� ![]() ���ֲ���
���ֲ���
B. 308Kʱ��HF�ĵ��볣��Ka>3.5��10-4
C. 298Kʱ����CaF2��Һ�м�������CaCl2��Ksp(CaF2)���С
D. 2HF(aq)+Ca2+(aq)![]() CaF2(s)+2H+(aq)K��0.68
CaF2(s)+2H+(aq)K��0.68
���𰸡�D
��������A����![]() =
=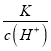 ��298Kʱ��������ˮϡ��HF��Һ��������Ũ�ȼ�С����
��298Kʱ��������ˮϡ��HF��Һ��������Ũ�ȼ�С����![]() ����A����B.298KʱK(HF)=3.5��10-4�������¶ȣ�ƽ�������ƶ�����Ka��3.5��10-4����B����C���¶Ȳ��䣬���ܶȻ����䣬��C����D����֪��HF(aq)H+(aq)+F-(aq)����CaF2(s)Ca2+(aq)+2F-(aq)��������2-�ڿɵ�2HF(aq)+Ca2+(aq)CaF2(s)+2H+(aq)����K=
����A����B.298KʱK(HF)=3.5��10-4�������¶ȣ�ƽ�������ƶ�����Ka��3.5��10-4����B����C���¶Ȳ��䣬���ܶȻ����䣬��C����D����֪��HF(aq)H+(aq)+F-(aq)����CaF2(s)Ca2+(aq)+2F-(aq)��������2-�ڿɵ�2HF(aq)+Ca2+(aq)CaF2(s)+2H+(aq)����K= ��0.68����D��ȷ����ѡD��
��0.68����D��ȷ����ѡD��


 ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�ֻ���Ļ��Ҫ�ɱ������������ز��Լ������Һ����ʾ����������ɡ������ǹ�ҵ���ñ�ϩ��A�����л���C��C7H6O3��Ϊԭ�Ϻϳ�Һ����ʾ�����ϣ�F������Ҫ���̣�
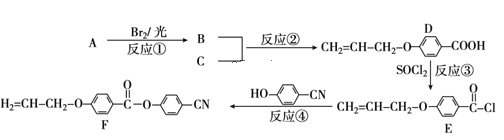
��1��������C�Ľṹ��ʽΪ___��B�Ĺ���������___��
��2������ת������������ȡ����Ӧ����___���Ӧ��ţ���
��3��д��B��NaOHˮ��Һ��Ӧ�Ļ�ѧ����ʽ___��
��4�����й��ڻ�����D��˵����ȷ����___������ĸ����
A.����������� B.1molD�������4molH2�����ӳɷ�Ӧ
C.һ�������·����Ӿ۷�Ӧ D.�˴Ź���������5���
��5��д���������������µĻ�����C��ͬ���칹��Ľṹ��ʽ___(��дһ��)��
�ٱ�����һ�����ֻ��2�� ���ܷ���������Ӧ �۱�������3��ȡ����
��6������������Ʊ����̣�д�����л���C����ϩΪԭ���Ʊ�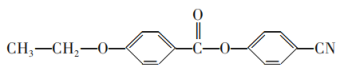 �ĺϳ�·������ͼ�����Լ����ã�___��
�ĺϳ�·������ͼ�����Լ����ã�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() �ķֽ��ܶ������ص�Ӱ�졣ʵ����
�ķֽ��ܶ������ص�Ӱ�졣ʵ����![]() ʱ��ͬ�����£�
ʱ��ͬ�����£�![]() Ũ����ʱ��仯��ͼ��ʾ������˵������ȷ����
Ũ����ʱ��仯��ͼ��ʾ������˵������ȷ����
A.ͼ�ױ���������������ͬʱ��![]() ��Ũ��ԽС����ֽ�����Խ��
��Ũ��ԽС����ֽ�����Խ��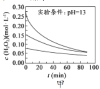
B.ͼ�ұ���������������ͬʱ����ҺpHԽС��![]() �ֽ�����Խ��
�ֽ�����Խ��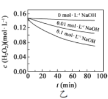
C.ͼ������������![]() ����ʱ����Һ����Խǿ��
����ʱ����Һ����Խǿ��![]() �ֽ�����Խ��
�ֽ�����Խ��
D.ͼ����ͼ��������������Һ�У�![]() ��
��![]() �ֽ����ʵ�Ӱ���
�ֽ����ʵ�Ӱ���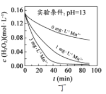
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���( )
A.��ѹ�����ںϳɰ��ķ�Ӧ
B.��H2��I2(g)��HI(g)������ɵ�ƽ����ϵ��ѹ����ɫ����
C.����ɫ��NO2����ѹ����ɫ�ȱ������dz
D.����ɫ����ˮ���պ���ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л������NaCl ��NaOH ��HCl ��NH4Cl ��CH3COONa ��CH3COOH ��NH3H2O ��H2O���ش��������⣮
��1��NH4Cl��Һ�����ԣ������ӷ���ʽ��ʾԭ�� ������Һ������Ũ�ȴ�С˳��Ϊ ��
��2�������£�pH=11��CH3COONa��Һ�У�ˮ���������c��OH����= ����pH=3��CH3COOH��Һ�У�ˮ���������c��H+��= ��
��3��������pH��������Ģ�NaOH�͢�NH3H2O�ֱ��ˮϡ��m����n����ϡ�ͺ�������Һ��pH����ȣ���m n�������������������=����
��4����ǰ������Һ�����ʵ���Ũ����ͬ��������ų���������ҺpH�ɴ�С��˳�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����һ�������£����淴Ӧ��aA(g)+bB(g)![]() cC(g)+dD(g)�ﵽƽ�⡣
cC(g)+dD(g)�ﵽƽ�⡣
�������������䣬�����¶ȣ�������Ӧ����________ (�����ӿ�����������������ͬ)���淴Ӧ����________�����´ﵽƽ���c���������ӣ�������ӦΪ_________(��������������������)��Ӧ��
��2����AlCl3��Һ���ɣ����գ����õ�����Ҫ���������_______���ѧʽ����
��3��pH = 3�Ĵ����pH = 11������������Һ�������Ϻ���Һ��________�����������������������������ԣ���Һ��c(Na��) ______c(CH3COO-) ������>������=������<������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.![]() ��ʾ���ȷ�Ӧ��
��ʾ���ȷ�Ӧ��![]() ��ʾ���ȷ�Ӧ
��ʾ���ȷ�Ӧ
B.�ڻ�ѧ��Ӧ�з������ʱ仯��ͬʱ����һ�����������仯
C.![]() �Ĵ�С���Ȼ�ѧ����ʽ�л�ѧ�������й�
�Ĵ�С���Ȼ�ѧ����ʽ�л�ѧ�������й�
D.�������ͷŵ����������ڷ�Ӧ�����յ�������ʱ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H��0��CO��H2O��Ũ�ȱ仯��ͼ��ʾ��
CO2(g)��H2(g) ��H��0��CO��H2O��Ũ�ȱ仯��ͼ��ʾ��
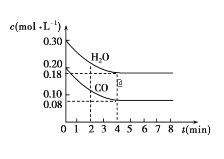
�������и��⣺
��1��0��4min�ڵ�ƽ����Ӧ����v(CO)��___mol/(L��min)��v(H2)��___mol/(L��min)��v(CO2)��___mol/(L��min)��
��2��������ͼ�б��CO2��H2��Ũ�ȱ仯��___
��3��T��(����850��)ʱ������ͬ�����з���������Ӧ�������ڸ����ʵ�Ũ�ȱ仯�����
ʱ��(min) | 0 | 2 | 3 | 4 | 5 | 6 |
CO | 0.200 | 0.138 | c1 | c1 | 0.116 | 0.096 |
H2O | 0.300 | 0.238 | c2 | c2 | 0.216 | 0.266 |
CO2 | 0 | 0.062 | c3 | c3 | 0.084 | 0.104 |
H2 | 0 | 0.062 | c4 | c4 |
�ٱ���3min��4min֮�䣬��Ӧ����___״̬��c1___0.08mol/L(����ڡ�����С�ڡ����ڡ�)��
�ڷ�Ӧ��4min��5min֮�䣬ƽ�����淴Ӧ�����ƶ������ܵ�ԭ����___(��ѡ)������5min��6min֮����ֵ�����仯�����ܵ�ԭ����___(��ѡ)��
a������ˮ���� b�������¶� c��ʹ�ô��� d����������Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������;�㷺�������ڸ�����������������Ҳ����Ϊ�Ʊ�������м��壮���������ף���������̼�����ϳɼ���Ƶķ�Ӧ���£�
![]() ��Ӧ1
��Ӧ1
��1����Ӧ��ϵ�д�����������������Ӧ
![]() ��Ӧ2
��Ӧ2
![]() ��Ӧ3
��Ӧ3
![]() ������̼������ֱ�Ӻϳɼ�����Ȼ�ѧ��Ӧ����ʽΪ ______ ��
������̼������ֱ�Ӻϳɼ�����Ȼ�ѧ��Ӧ����ʽΪ ______ ��
![]() Ϊ�˸����������ɼ���ƣ�Ӧѡ��ķ�Ӧ�����ǽϵ͵��¶Ⱥ� ______
Ϊ�˸����������ɼ���ƣ�Ӧѡ��ķ�Ӧ�����ǽϵ͵��¶Ⱥ� ______ ![]() ����
����![]() ��
��
A.����![]() ��ѹ
��ѹ![]() ��ѹ
��ѹ
��2����ͼ1�Ƿ�Ӧ2�ͷ�Ӧ3��lnK���¶�T�Ĺ�ϵ��ͬһ����ʱ��Ӧ2��K ______ ![]() ��������������С����
��������������С����![]() ��Ӧ3��K������� ______
��Ӧ3��K������� ______ ![]() ������Ӧ2��������Ӧ3��
������Ӧ2��������Ӧ3��![]() �����ģ�
�����ģ�
��3�����������Ƴ�ʼ�ܶ�Ϊ![]() ��CO�ķ�ѹΪ
��CO�ķ�ѹΪ![]() �����´���Ӧ������������ת����
�����´���Ӧ������������ת����![]() Ϊ���꣬ʱ��Ϊ������õ���ͼ2��
Ϊ���꣬ʱ��Ϊ������õ���ͼ2��

![]() ����ͼ��ѡ����ʵķ�Ӧ�¶� ______ �������� ______ ��
����ͼ��ѡ����ʵķ�Ӧ�¶� ______ �������� ______ ��
![]() ��
��![]() Ϊ
Ϊ![]() ʱ�������м������̼��Ƶ�������Ϊ50��1������������ ______
ʱ�������м������̼��Ƶ�������Ϊ50��1������������ ______ ![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com