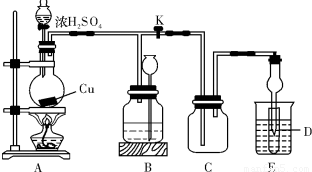
附中某化学兴趣小组为探索铜跟浓硫酸的反应,用下图所示装置进行有关实验.
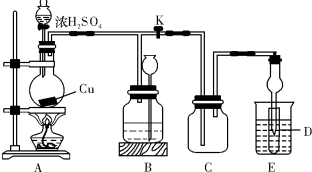
郝欣同学取a g Cu片12mL18mol/L浓H
2SO
4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H
2SO
4和Cu剩余.
请回答:
(1)请写出Cu与浓H
2SO
4反应的化学方程式
Cu+2H
2SO
4(浓)CuSO
4+2H
2O+SO
2↑
Cu+2H
2SO
4(浓)CuSO
4+2H
2O+SO
2↑
.装置E中试管D内盛品红溶液,当C中气体集满,D中有可能观察到的现象是
品红溶液褪色
品红溶液褪色
.
(2)装置B的作用是贮存多余的气体.当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于作热的作用,A处仍有气体产生,此时B中现象是
试剂瓶中液面下降,长颈漏斗中液面上升
试剂瓶中液面下降,长颈漏斗中液面上升
.B中应放置的液体:
D
D
(填字母).
A.饱和Na
2SO
3溶液 B.酸性KMnO
4 C.浓溴水 D.饱和NaHSO
3溶液
(3)下列药品中,能够证明反应后的烧瓶中有酸剩余的是
AD
AD
.
A.Fe粉 B.BaCl
2溶液 C.Ag D.饱和NaHSO
3溶液
(4)小明同学向A中反应后的溶液中通入氧气,发现铜片全部溶液,且仅生成硫酸铜溶液该化学反应方程式是
2Cu+O2+2H2SO4═2CuSO4+2H2O;
2Cu+O2+2H2SO4═2CuSO4+2H2O;
.




 阅读快车系列答案
阅读快车系列答案