
【题目】单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X为Z的氧化物,Y为氢化物,分子结构与甲烷相似,回答下列问题:
![]()
(1)能与X发生化学反应的酸是________,由X制备Mg2Z的化学方程式为:____________。
(2)由Mg2Z生成Y的化学反应方程式为_______________,Y分子的电子式为__________。
(3)Z、X中共价键的类型分别是____________。
【答案】(1)氢氟酸;SiO2+MgO2↑+Mg2Si
(2)Mg2Si+4HCl=2MgCl2+SiH4;
(3)非极性键、极性键
【解析】试题分析:单质Z是一种常见的半导体材料,则Z为Si,X为Z的氧化物,则X为SiO2,Y为氢化物,分子结构与甲烷相似,则Y为SiH4,加热SiH4分解得到Si与氢气。(1)能与SiO2发生化学反应的酸是氢氟酸;由SiO2制备Mg2Si的化学方程式为:SiO2+4Mg![]() 2MgO+Mg2Si。
2MgO+Mg2Si。
(2)由Mg2Z生成Y的化学反应方程式为:Mg2Si+4HCl="2" MgCl2+SiH4↑,Y为SiH4,电子式为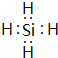 。
。
(3)Z为Si,周期表中位于第三周期IVA族,其单质属于原子晶体,化学键类型为非极性共价键;X为SiO2,属于原子晶体,含有的化学键属于极性共价键。


科目:高中化学 来源: 题型:
【题目】现有如下仪器,仪器中已注入溶液,回答下列问题。
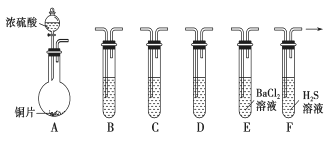
(1)加热装置A,写出铜与浓硫酸反应的化学方程式:_______________________________
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________、C________、D________。能说明碳的非金属性比硅强的实验现象是_________________。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是________________,反应方程式为________________。
②若证明SO2具有还原性,在E中采取的实验操作为_________________________________,
其实验现象为__________________,反应原理为__________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个丰富的资宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和________________池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用:_______________________ (写一点即可)。
(2)电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
①海水不能直接通人到阴极室中,理由是_____________________。
②A口排出的是__________________(填“淡水”或“浓水”)。
(3)用苦卤(含 Na+、K+、Mg2+ Cl-、Br-等离子)可提取溴,其生产流程如下: 
①若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为:____________________.
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化重新获得含Br2的溶液?______________。
③向蒸馏塔中通人水蒸气加热,控制温度在90°C左右进行蒸馏的原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备硫酸常用接触法,工业上制硝酸常用氨的催化氧化法。下列关于工业上制硫酸与硝酸的说法中不正确的是( )
A. 在沸腾炉中进行的反应为:4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
B. 工业上制硫酸与硝酸都用到同一工艺设备:吸收塔
C. 硫酸工业、硝酸工业都需要对工业尾气进行处理
D. 工业上制备硫酸和制硝酸涉及的反应都属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于中和热测定实验,下列说法不正确的是
A.烧杯间填满碎泡沫塑料是为了减少实验过程中的热量损失
B.使用环形玻璃搅拌棒既可以搅拌又可以避免损坏温度计
C.向盛装酸溶液的烧杯中加碱溶液时要小心缓慢
D.测过酸的温度计要用水清洗后再测碱的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种生命元素,组成某些蛋白质时离不开它。SO2是硫的一种重要氧化物,为探究SO2的性质,某化学兴趣小组的同学进行如下系列实验:
(1)将SO2通入紫色石蕊试液,现象是_________________。
(2)将SO2通入FeCl3溶液中,使其充分反应。写出SO2与FeCl3反应的离子方程式___________________;为了验证SO2与FeCl3发生了氧化还原反应,将反应后的溶液分成两份,并设计如下实验:
方案1:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案2:往第二份试液中加入KSCN溶液,不变红,再加入新制氯水,溶液变红。
上述方案合理的是__________。(填“方案1”或“方案2”或“均合理”)
(3)将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀。为探究该白色沉淀的成分,他们设计了如下实验流程:

操作①的名称为_____,试剂A为_______:加入试剂A后,白色沉淀未见溶解,则该白色沉淀的成分是_______(填化学式)。
(4)为探究SO2的漂白是SO2直接作用于有色物质还是SO2与水反应的产物的作用。设计如图装置进行探究。
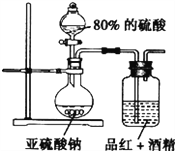
(信息提示:品红能溶解在酒精中形成红色溶液;H2SO3是二元弱酸)
①亚硫酸钠和浓硫酸反应的化学方程式为__________。
②请指出设计的装置中两个明显的不足:
___________________;________________________。
③按照修改后的装置,实验中控制SO2以较缓慢的速率通过品红的酒精溶液,60分钟后溶液仍不褪色,由此可推断,引起品红褪色的微粒可能是______________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别食盐水和蔗糖水的方法有:①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热;②测量溶液的导电性;③将溶液与溴水混合、振荡;④观察溶液颜色。其中在实验室进行鉴别的正确方法是
A. ①② B. ①③ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。
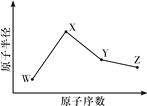
(1)X位于元素周期表中的位置是____________________。
(2)Z的气态氢化物和溴化氢相比,较稳定的是____________(写化学式)。
(3)W与X形成的一种化合物和水反应能生成W的单质,请写出该反应的化学方程式:________________________________________________________________________。
(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com