
【题目】某温度下,在2L的密闭容器中,加入1mol X(g)和2mol Y(g)发生反应:X(g)+mY (g)3Z(g)△H<0,平衡时,X和Y的转化率都是10%.下列叙述不正确的是( )
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45molL﹣1
【答案】CD
【解析】解:A.如果各反应物的物质的量之比等于其计量数之比,则反应物的转化率相等,该反应中X、Y的转化率相等,说明加入的X、Y的物质的量之比等于其计量数之比=1mol:2mol=1:m,m=2,故A正确; B.达到平衡时X、Y的转化率都是10%,则参加反应的n(X)=1mol×10%=0.1mol,生成的n(Z)=3n(X)(反应)=3×0.1mol=0.3mol,反应前后气体计量数之和不变,则反应前后气体总物质的量不变,相同条件下,气体的体积分数等于其物质的量分数= ![]() ×100%=10%,故B正确;
×100%=10%,故B正确;
C.恒容条件下,升高温度平衡逆向移动,但气体总物质的量不变,所以压强不变,故C错误;
D.将平衡后的容器体积压缩至1L,增大压强平衡不移动,X的物质的量不变为1mol×(1﹣10%)=0.9mol,其浓度= ![]() =0.9mol/L,故D错误;
=0.9mol/L,故D错误;
故选CD.
【考点精析】通过灵活运用化学平衡的计算,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%即可以解答此题.


科目:高中化学 来源: 题型:
【题目】A、B、C是单质,其中A是金属,各种物质间的转化关系如图:
根据图示转化关系回答:
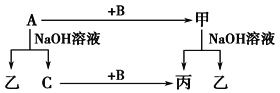
(1)写出下列物质的化学式。
A________,B________,甲_________,乙________。
(2)写出下列变化的化学方程式。
①A与NaOH溶液反应的化学方程式________________________________。
②甲与NaOH溶液反应的离子方程式________________________________。
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________,转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是中学化学实验室的常见药品,回答下列实验问题。
Ⅰ.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435ml。同学们发现实验室内没有450ml的容量瓶,某同学提议用1个200ml容量瓶和1个250ml容量瓶来配制,你认为该提议_________(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/ml、98%的浓硫酸________ml。

Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(1)图中盛装浓硫酸的仪器名称为________________。
(2)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是SO2,①、②、③处发生的变化分别说明SO2具有_____________、_____________和_____________(填SO2表现出的性质)。
(3)打开活塞K,a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位置的滤纸滴加______________溶液,该试剂的作用是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法中正确的是( )
A.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
B.由2H和18O所组成的水11 g,其中所含的中子数为4NA
C.常温下丁烯和环丙烷组成的42 g混合气体中H原子数为6NA
D.1 mol FeI2与足量氯气反应时转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬铁矿的主要成分可表示为FeOCr2O3 , 还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钠(Na2Cr2O7)的过程如图所示: 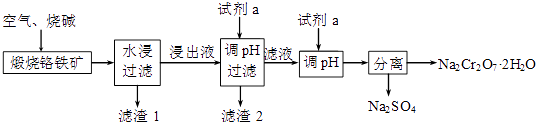
已知:①NaFeO2在水溶液中强烈水解生成对应的氢氧化物.
②2CrO ![]() +2H+Cr2O
+2H+Cr2O ![]() +H2O
+H2O
(1)完成煅烧过程中铬铁矿发生的主要反应的化学方程式:
FeOCr2O3+7O2+ ![]() Na2CrO4+NaFeO2+
Na2CrO4+NaFeO2+
上述反应中每熔化1mol FeOCr2O3 , 转移的电子数为
(2)浸出液的成分除Na2CrO4、NaOH外,还含有(写化学式,下同),滤渣1的成分是 .
(3)调节浸出液pH所加的试剂a是(写化学式).
(4)该流程中用了两步调节pH,若合并成一步调pH,酸性过强,产品Na2Cr2O7晶体中可能含有较多杂质,用离子方程式说明引入该杂质的原因 .
(5)100kg铬铁矿(含FeOCr2O3 89.6%)最多可获得Na2Cr2O72H2O的质量为kg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 蔗糖和麦芽糖均为双糖
B. 酶是一类具有高选择催化性能的蛋白质
C. 植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色
D. 淀粉和纤维素水解的最终产物均为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项有机化合物的命名或分类正确的是( )
A.2,3﹣二甲基﹣2﹣乙基己烷
B.CH3CH2CH2Cl 氯丙烷
C.![]() 属于芳香化合物
属于芳香化合物
D.![]() 属于羧酸
属于羧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下各组离子因发生氧化还原反应而不能大量共存的是( )
A. Ca2+、H+、SO42-、HCO3-B. H+、Fe2+、SO42-、 NO3-
C. Na+、Cu2+、Cl-、S2-D. Fe3+、K+、SCN-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com