
【题目】短周期元素X、Y、Z组成的化合物Y2X和ZX2。Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3。已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答:
(1)X、Y、Z元素的名称及符号_________、___________、____________。
(2)写出ZX2的化学式______________。
(3)写出Y2X对应水化物的电子式_________,并指出其中存在的化学键___________________。
(4)写出Y2X溶于水的溶液与ZX2反应的化学方程式_______________________________。
【答案】氧(O) 钠(Na) 碳(C) CO2 ![]() 离子键和极性共价键 2NaOH+CO2===Na2CO3+H2O或CO2+NaOH===NaHCO3
离子键和极性共价键 2NaOH+CO2===Na2CO3+H2O或CO2+NaOH===NaHCO3
【解析】
根据Z原子的最外层电子数是次外层电子数的2倍,利用原子核外电子排布的规律,可判断出Z原子只有两个电子层,K层为2个电子,L层(即最外层)为4个电子,由此可得出Z原子的原子序数为6,为碳元素;再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,列式计算出元素的质子数,推出X、Y为何种元素,然后利用单质及化合物的性质来解答。
由Z原子的最外层电子数是次外层电子数的2倍,则Z为两个电子层时,推出Z为碳元素,再由三种元素原子的电子总数为25,且Z与Y的原子序数之和比X的原子序数的2倍还多1,则设X原子的质子数为x,Y原子的质子数为y,根据题意,可得出以下关系:
6+x+y=25,6+y=2x+1,解得:x=8,y=11,即X为氧元素,Y为钠元素。
(1)由上述分析可知,X为氧元素(O),Y为钠元素(Na),Z为碳元素(C),
故答案为:氧(O);钠(Na);碳(C)。
(2)ZX2是CO2,故答案为:CO2。
(3)Y2X为Na2O,对应水化物为NaOH,NaOH是离子化合物,由钠离子与氢氧根离子构成,氢氧化钠电子式为![]() ;钠离子与氢氧根离子之间为离子键,氢氧根离子中氢原子与氧原子之间为共价键,
;钠离子与氢氧根离子之间为离子键,氢氧根离子中氢原子与氧原子之间为共价键,
故答案为:![]() ;离子键、共价键。
;离子键、共价键。
(4)Y2X为Na2O,溶于水得NaOH溶液,ZX2是CO2,CO2与NaOH溶液反应生成碳酸钠与水,反应方程式为2NaOH+CO2=Na2CO3+H2O或CO2+NaOH=NaHCO3,
故答案为:2NaOH+CO2=Na2CO3+H2O或CO2+NaOH=NaHCO3。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列反应为放热反应的( )
①CaCO3分解 ②钠与水反应 ③硫在O2中燃烧 ④8个结晶水的氢氧化钡与氯化铵的反应 ⑤CaO+H2O=Ca(OH)2 ⑥N2与H2合成NH3 ⑦NaOH和CH3COOH的反应
A. ①②③B. ④⑤⑦C. ④⑦⑧D. ②③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于消去反应的是( )
①CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
②2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
③CH3CH2CH2Br![]() CH3CH===CH2↑+HBr
CH3CH===CH2↑+HBr
④2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
⑤CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
⑥![]()
⑦CH3CH2OH![]() CH2===CH2↑+H2O
CH2===CH2↑+H2O
⑧CH3CH2OH+HCOOH![]() HCOOCH2CH3+H2O
HCOOCH2CH3+H2O
A. ⑤⑦⑧ B. ②③ C. ③④⑤ D. ③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构简式可进一步简化,如:
CH3CH2CH2CH3: 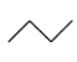 ,
,![]() :
: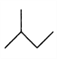 ,CH3CH=CHCH3 :
,CH3CH=CHCH3 :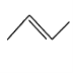
(1)写出下列有机物的结构简式:
2,2,3,3-四甲基戊烷:____________________;
3,4-二甲基-4-乙基庚烷:____________________。
(2)写出下列物质的分子式:
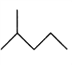 :__________________________;
:__________________________;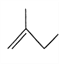 :__________________________。
:__________________________。
(3)用系统命名法命名下列物质:
![]() ____________________。
____________________。
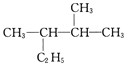 ____________________。
____________________。
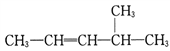 ____________________。
____________________。
![]() ____________________。
____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中,钢铁与食盐水接触,发生吸氧腐蚀,在负极上发生的电极反应是( )
A. Fe-2e-=Fe2+B. 2H++2e-=H2↑
C. Na++e-=NaD. 2H2O+O2+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示晶体结构是一种具有优良的电压、电光等功能的晶体材料的最小结构单元(晶胞).晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是(各元素所带电荷均已略去)( )
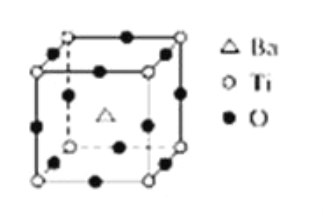
A. 8;BaTi8O12
B. 8;BaTi4O9
C. 6;BaTiO3
D. 3;BaTi2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如下表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 原子核电荷数是内层电子数的4倍 |
C | 1molC单质能与冷水反应,在标准状况下生成11.2L H2 |
D | 原子最外层电子数等于其周期序数 |
E | 负二价阴离子的电子层结构与Ar原子相同 |
(1)E的简单离子的结构示意图为____________;
(2)C元素和A元素能化合形成C3A的化合物,该化合物化学式是__________;
(3)C和D简单离子的半径大小为____ >_____;(用离子符号表示)
(4)用两根玻璃棒分别蘸取A元素最高价氧化物对应水化物的浓溶液和A元素的氢化物的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 _____________________________ 。
(5)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中可行的是_________(填序号);
a.比较两种单质的颜色 b. 依据两元素在周期表中的位置
c.比较氢化物的稳定性 d.依据两元素单质在自然界中的存在状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10mLNO、CO2的混合气体通过足量的Na2O2后,气体的体积变为5mL(相同状况),则CO2和NO的体积比不可能为
A. 1∶1 B. 1∶2
C. 2∶1 D. 3∶2
【答案】B
【解析】
NO、CO2的混合气体通过足量的Na2O2发生反应有2Na2O2+2CO2═2Na2CO3+O2、2NO+O2═2NO2,问题的关键在于NO与氧气反应存在着三种可能性,一种情况是恰好反应,一种情况是NO过量,另一种情况可能是O2过量,据此讨论计算。
NO、CO2的混合气体通过足量的Na2O2发生反应有(1)2Na2O2+2CO2═2Na2CO3+O2、(2)2NO+O2═2NO2,假设参加反应的CO2为x mL,NO为ymL,则x+y=10,由方程式得以下关系:
①2CO2+ 2Na2O2= 2Na2CO3+ O2
2mL 1mL
xmL ![]() mL
mL
②2NO + O2 = 2NO2
2mL 1mL 2mL
ymL ![]() mL
mL
当反应②恰好反应时,即当y=x时(此时x、y都等于5),生成的NO2的体积为5mL,显然符合题意,A正确;当y>x时,NO有过量,O2反应完,此时反应掉的NO为xmL,则剩余的NO为(ymL-xmL),生成的NO2气体为xmL,因此反应最后得到的混合气体为NO和NO2,其体积和为(ymL-xmL)+xmL=ymL,结合x+y=10,再根据NO过量的前提条件为y>x,可以得出结论y>5,这与题意“气体体积缩小为5mL”不符,B错误;当y<x时,NO不足,O2过量,此时反应掉的O2为![]() mL,剩余的O2为(
mL,剩余的O2为(![]() —
—![]() )mL,生成的NO2气体为ymL,因此,反应最后得到的混合气体为O2和NO2,其体积和为:(
)mL,生成的NO2气体为ymL,因此,反应最后得到的混合气体为O2和NO2,其体积和为:(![]() —
—![]() )mL+ymL=5mL,这与题意“气体体积缩小为5mL”符合,这表明如果y<x,这种情况都能符合题意,C、D正确,故选B。
)mL+ymL=5mL,这与题意“气体体积缩小为5mL”符合,这表明如果y<x,这种情况都能符合题意,C、D正确,故选B。
【点睛】
本题考查混合物的有关计算,属于讨论型计算,侧重对综合能力的考查,确定反应可能的情况是解答的关键。
【题型】单选题
【结束】
24
【题目】在一定温度和压强下,将一支容积为21mL的试管充满NO2后,倒置于一个盛水的水槽中,当试管内液面上升一定高度不再变化时,在相同条件下再通入O2,若要使试管内的液面仍保持在原高度,则通入O2的体积为
A. 8.75mL B. 12.25mL
C. 5.25mL D. 10.5mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com