
【题目】过氧化钠与二氧化碳能生成氧气,在潜水艇中做制氧剂。某学生为了验证这一实验,利用足量的大理石、盐酸和1.95g Na2O2,制取O2。设计出如下图实验装置
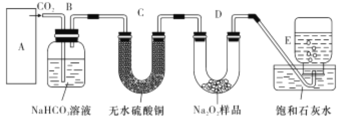
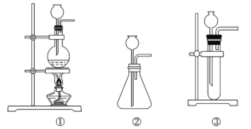
(1)A中制取CO2的图,应选用________(填①或②或③)
写出本题中制取氧气的化学方程式__________________B装置的作用是___________________
(2)若E中的出现少量白色沉淀,说明原因:__________________________________
(3)若D中1.95g Na2O2接近反应完毕时,预测会有何种现象:_______________________
【答案】② 2Na2O2+2CO2=2Na2CO3+ O2 除去CO2中混有的HCl气体 CO2并未全部与Na2O2反应,少许溢出使石灰水变浑浊,E中石灰水浑浊明显增加 集气瓶内液面不再下降
【解析】
(1)A中制取CO2的图,制取二氧化碳是用大理石和盐酸反应,不需要加热,该反应是放热反应,应该用比较大的容器反应;用过氧化钠和二氧化碳的反应,用饱和碳酸氢钠溶液吸收二氧化碳中的氯化氢气体。
(2)二氧化碳未完全反应则可能会使澄清石灰水变浑浊。
(3)当过氧化钠接近反应完,则集气瓶内液面不再下降。
(1)A中制取CO2的图,制取二氧化碳是用大理石和盐酸反应,不需要加热,该反应是放热反应,应该用比较大的容器反应,应选用②,制取氧气主要是二氧化碳和过氧化钠反应,其化学方程式2Na2O2+2CO2=2Na2CO3+ O2,B装置的作用是主要是除掉二氧化碳中的氯化氢,故答案为:②;2Na2O2+2CO2=2Na2CO3+ O2;除掉二氧化碳中的氯化氢。
(2)若E中的出现少量白色沉淀,说明原因CO2并未全部与Na2O2反应,少许溢出使石灰水变浑浊,故答案为:CO2并未全部与Na2O2反应,少许溢出使石灰水变浑浊。
(3)若D中1.95g Na2O2接近反应完毕时,不再生成氧气,出来的二氧化碳和澄清石灰水反应,因此出现集气瓶内液面不再下降,溶液变浑浊,故答案为:集气瓶内液面不再下降。


科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,取甲、乙、丙各30.0mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不发生变化):请回答:
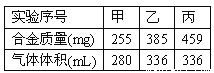
①甲组实验中,盐酸(选填“过量”、“适量”或“不足量”,下同)___,乙组实验中盐酸___。
②盐酸的物质的量浓度为___。
③合金中Mg、Al的物质的量之比为___。
(2)甲、乙两烧杯中各盛1L0.6mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体的体积比V(甲):V(乙)=3:4,则加入铝粉的质量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述错误的是( )注:氨气在水中溶解度(体积比——V水:V气=
1:700,CO2在水中溶解度1:1。

A.A气体是NH3,B气体是CO2
B.侯氏制碱法的工艺流程应用了物质溶解度的差异
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用图示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
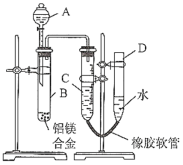
(1)A中试剂为__________________
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是_______________________________
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂。上述操作的顺序是_______________________(填序号)。
(4)B中发生反应的化学方程式为_____________________________________________________
(5)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式书写错误的是( )
A.NaHCO3水解的离子方程式:HCO3-+ H2O![]() CO32-+H3O+
CO32-+H3O+
B.NH4Cl水解的化学方程式:NH4Cl+H2O![]() NH3·H2O+HCl
NH3·H2O+HCl
C.Al(OH)3的两性电离方程式:H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH
Al3++3OH
D.NaHSO3的电离方程式:NaHSO3=Na++HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图所示的实验装置中各部分仪器的主要作用的叙述正确的是( )

A.大烧杯d:防止在a发生破裂后使药品外溢
B.量气管b:读出反应前后与水面相平的刻度
C.水准管c:可方便地向整个装置中添加液体
D.温度计e:搅拌烧杯中的液体并且测量温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了如下图装置,反应完毕,电解质溶液的pH保持不变。下列说法正确的是
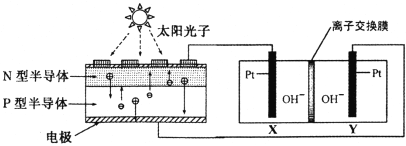
A. 图中N型半导体为正极,P型半导体为负极
B. Y 电极的反应:4OH--4e-=2H2O +O2↑
C. 图中离子交换膜为阳离子交换膜
D. 该装置实现了“太阳能→化学能→电能”的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)在该反应中,HCl表现的性质有______、________.
①MnO2 +4HCl(浓)![]() Cl2↑+ MnCl2+ 2H2O
Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为________(填化学式),被氧化物质的物质的量为 _____,同时转移电子数为_____(用NA表示)。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_________,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______。
(4)②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____。
(5)已知反应4HCl(g)+O2  2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
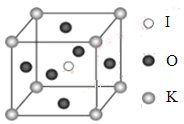
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com