
【题目】已知某“84消毒液”瓶体部分标签如图所示,已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比) 后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为_____mol·L-1。
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是______(填字母)。
A.溶液中NaClO的物质的量 B.溶液的浓度 C.溶液中NaClO的摩尔质量 D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。回答下列问题。
①如图所示的仪器中,有些是不需要,配制上述溶液还需要_____________玻璃仪器
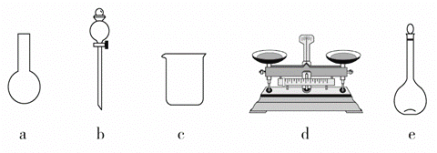
②需要称量NaClO固体的质量为_______ g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g·cm-3)的浓硫酸配制230mL 2.3mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________ mL。
③若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
【答案】4.0 A 玻璃棒、胶头滴管 149.0 4.6 31.25 D
【解析】
(1)根据![]() 计算该“84消毒液”的物质的量浓度;
计算该“84消毒液”的物质的量浓度;
(2)根据该物理量是否与溶液的体积有关判断;
(3)①根据配制溶液的步骤判断需要的仪器;
②配制480mL含NaClO质量分数为25%的溶液,需要用500mL容量瓶,利用500mL计算所需次氯酸钠的质量;
(4)硫酸是强电解质,氢离子浓度是硫酸浓度的2倍;
②根据稀释前后硫酸的质量不变计算浓硫酸的体积,需用250 mL容量瓶配制该稀硫酸;
③根据![]() 判断误差。
判断误差。
(1)该“84消毒液”的物质的量浓度![]() 4.0mol·L-1;
4.0mol·L-1;
(2)A.溶液中NaClO的物质的量=cV,所以与溶液的体积有关,A正确;
B.溶液的浓度![]() ,与溶液的体积无关,B错误;
,与溶液的体积无关,B错误;
C.NaClO的摩尔质量的数值等于相对分子质量,所以与溶液的体积无关,C错误;
D.溶液的密度与溶液的体积无关,D错误;
故选A;
(3)①配制该溶液需要用托盘天平称取次氯酸钠,在烧杯中溶解,然后转移到500 mL容量瓶中,并用胶头滴管定容,需要的仪器是托盘天平、烧杯、玻璃棒、500 mL容量瓶、胶头滴管,缺少的仪器是玻璃棒、胶头滴管;
②配制480mL含NaClO质量分数为25%的溶液,需要用500 mL容量瓶,m(NaClO)= 4.0mol·L-1×0.5L×74.5g/mol=149.0g;
(4)①硫酸是强电解质,氢离子浓度是硫酸浓度的2倍,所以2.3 mol·L-1的稀硫酸中,H+的物质的量浓度为4.6mol·L-1;
②需用250mL容量瓶配制该稀硫酸,设需要浓硫酸的体积是V mL,250 mL× 2.3 mol·L-1×98g/mol=V mL×1.84g·cm-3×98%,解得V=31.25mL;
③A.配制前,容量瓶中有少量蒸馏水,所配制的稀硫酸浓度无影响,A错误;
B.量取浓硫酸时,仰视液体的凹液面,浓硫酸体积偏大,所配制的稀硫酸浓度偏大,故B错误;
C.未冷却,立即转移至容量瓶定容,所配溶液体积偏小,所配制的稀硫酸浓度偏大,故C错误;
D.定容时,仰视溶液的凹液面,所配溶液体积偏大,所配制的稀硫酸浓度偏小,D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】下表中是元素周期表的一部分,①~⑦分别表示元素周期表中对应位置的元素。
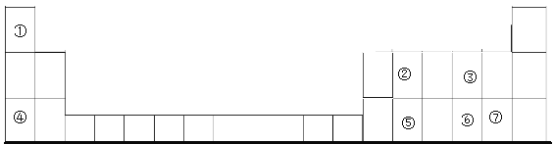
(1)元素⑤在周期表中的位置是___。
(2)元素①和⑥形成最简单化合物的电子式是___。元素②和③形成的一种化合物是造成温室效应的主要成分,该化合物的结构式为___。
(3)元素③和⑤形成的晶体属于___晶体。
(4)化合物A和化合物B均由元素①、③、④、⑥四种元素组成,它们的水溶液能互相反应,反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,可用离子方程式![]() +
+![]() =
=![]() 表示的是
表示的是
A.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
B.Mg(OH)2+2HCl=MgCl2+2H2O
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B. 从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C. 配制500mL 0.1mol/L的CuSO4溶液,需8.0g硫酸铜固体
D. 0.1mol/L MgCl2溶液中Cl-物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知浓硫酸的密度是1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%。取10mL浓硫酸和a mL水混合得到溶液的物质的量浓度为c mol/L,质量分数为b%。下列组合正确的是( )
(1)若c=9.2,则a<18.4,b>49 (2)若c=9.2,则a<18.4,b<49
(3)若b=49,则a=18.4,c<9.2 (4)若b=49,则a=18.4,c>9.2。
A.(1)(3)B.(1)(4)C.(2)(3)D.(2)(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示图像中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,按题给信息将相应图的字母填入下列空格中,并写出所发生反应的离子方程式。
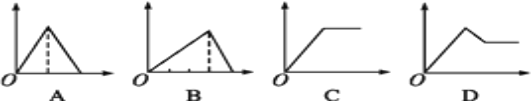
(1)表示向饱和AlCl3溶液中滴加氨水至过量的图像是_____(填字母,下同)
(2)表示向饱和AlCl3溶液中滴加NaOH溶液至过量的图像是_____。
(3)表示向饱和石灰水中通入CO2至过量的图像是_____。
(4)表示向MgCl2和AlCl3的混合溶液中滴加NaOH溶液至过量的图像是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如CH3CH=CHCH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A. X的化学式为C8H8
B. 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C. X能使酸性高锰酸钾溶液褪色
D. X与足量的H2在一定条件下反应可生成饱和烃Z, Z的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科
(1)从氯化钾溶液中得到氯化钾固体,常用的方法是______________。
(2)从碘水中分离出碘,实验方法的名称为____________,该方法主要实验仪器是____。
(3)现有A、B两种有机物的液态混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃。回答下列问题:
①分离上述A、B的混合物,常用的方法是______;
②如图是某同学设计的分离A、B混合物的操作示意图,请在其冷凝管处标上进出水方向(用箭头↑表示)______;蒸馏烧瓶内碎瓷片的作用是______。
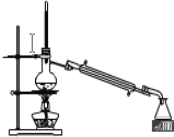
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,其合成及应用一直备受广大化学工作者的关注。N2和H2生成NH3的反应为:N2(g)+3H2(g)![]() 2NH3(g) △H=-92kJmol-1。
2NH3(g) △H=-92kJmol-1。
(1)已知:N2(g)![]() 2N(g) ; H2(g)
2N(g) ; H2(g)![]() 2H(g),则断开1 mol N-H键所需要的能量是_____________kJ。
2H(g),则断开1 mol N-H键所需要的能量是_____________kJ。
(2)有利于提高合成氨平衡产率的条件是_______________。
A. 低温 B.高温 C.低压 D.高压 E.催化剂
(3)向一个恒温恒压容器充入1 mol N2和3mol H2模拟合成氨反应,下图为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。
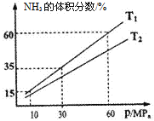
若体系在T1、60MPa下达到平衡。
①此时平衡常数Kp_______(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留3位小数)。
②T1_____________T2(填“>”、“<”或“=”)。
(4)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步 N2(g) ![]() 2N*;H2(g)
2N*;H2(g) ![]() 2H*(慢反应)
2H*(慢反应)
第二步 N*+H* ![]() NH*;NH*+H*
NH*;NH*+H* ![]() NH2*;NH2* +H*
NH2*;NH2* +H* ![]() NH3*;(快反应)
NH3*;(快反应)
第三步 NH3* ![]() NH3(g) (快反应)
NH3(g) (快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1__________E2(填“>”、“<”或“=”),判断理由是________________________________________________。
(5)肼(N2H4)又称为联氨,可作火箭发动机的燃料。肼分子的电子式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com