
【题目】下列物质的制备与工业生产实际相符的是( )
①![]()
②饱和![]()
③浓盐酸![]()
④![]()
⑤![]()
⑥铝土矿![]()
A.①④⑤B.②④⑥C.②③⑤⑥D.①②③④⑤⑥
【答案】B
【解析】
①工业用氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,故①错误;
②联合制碱法的工业流程为:先向饱和食盐水中通入![]() ,再通入
,再通入![]() 气体,析出
气体,析出![]() 晶体,然后碳酸氢钠在加热的条件下生成碳酸钠,故②正确;
晶体,然后碳酸氢钠在加热的条件下生成碳酸钠,故②正确;
③工业上制备漂白粉的工业流程是:通过电解饱和食盐水生成氯气,然后将氯气通入石灰乳制取漂白粉,故③错误;
④工业上是通过煅烧硫铁矿生成二氧化硫,然后将二氧化硫氧化生成三氧化硫,最后用水(浓硫酸)吸收生成硫酸,故④正确;
⑤工业上制Mg的工业流程为:MgCl2溶液蒸发结晶得到MgCl26H2O ,再在氯化氢气氛中得到无水MgCl2 ,最后电解熔融的氯化镁得到Mg,故⑤错误;
⑥工业制铝流程为:铝土矿用氢氧化钠溶解得到NaAlO2溶液,在偏铝酸钠溶液中通入二氧化碳得到Al(OH)3 ,将氢氧化铝加热分解生成氧化铝,最后电解熔融的氧化铝得到铝,故⑥正确;
正确的有②④⑥,故选B。


科目:高中化学 来源: 题型:
【题目】关于化学反应的方向,下列说法错误的是( )
A.在温度、压强一定的条件下,焓与熵因素共同决定一个化学反应的方向
B.温度、压强一定时,放热的熵增加反应 一定能自发进行
C.反应![]() △H < 0,低温有利于反应自发进行
△H < 0,低温有利于反应自发进行
D.固体溶解过程与焓变有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是:
A. 在一个氧化还原反应中,氧化剂的氧化性强于氧化产物
B. 在一个氧化还原反应中,还原产物的还原性弱于还原剂
C. amolH2SO4中,含有b个氧原子,则阿伏加德罗常数可以表示为b/4a/mol
D. 配制0.05mol/LNa2CO3溶液90mL,需Na2CO3固体5.3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】平昌冬奥会“北京8 分钟”主创团队用石墨烯制作了-20℃能发热4 h 的智能服饰; 用铝合金管材和碳纤维制作了高2.35m、重量仅为10kg 的熊猫木偶,向世界展现了新时代的中国形象。下列说法中,不正确的是

A. 石墨烯是能导热的金属材料 B. 铝合金是密度较低的金属材料
C. 碳纤维是耐低温的无机非金属材料 D. 新型材料种类多、用途广
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A. KClO3+6HC1=KCl+3C12↑+3H2O 中,生成13.44L (标准状况) C12转移电子数为1.2 NA
B. 标准状况下,22.4LC12通入足量水中转移电子数为NA
C. 足量的MnO2与一定量的浓盐酸反应得到1mol Cl2,若向反应后的溶液中加入足量的AgNO3,则生成AgC1的物质的量为2 mol
D. 5.6g Fe 与一定量的稀硝酸反应,转移电子数可能为0.26 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是一种与人类生活最密切的物质之一。以食盐为原料可以制取金属钠、氯气、氢气、烧碱等宝贵的化学用品和化工原料。
(1)写出工业制备金属钠的化学方程式:________。
(2)电解________可制得烧碱、氢气和氯气,这称为________工业。写出该工业中的电极反应式及总反应式:阳极_________;阴极________;总反应式________。
(3)我国著名的化工专家侯德榜发明的“联合制碱”法也以食盐为基础原料,该方法为先向饱和食盐水中通入![]() ,再通入
,再通入![]() 气体,析出
气体,析出![]() 晶体,化学方程式为________;将析出的
晶体,化学方程式为________;将析出的![]() 晶体灼烧即得纯碱,化学方程式为___________。
晶体灼烧即得纯碱,化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法中正确的是( )
①仅用试管、胶头滴管、溴水、KI淀粉溶液就可比较Br2与I2的氧化性的强弱
②利用烧杯、玻璃棒、胶头滴管、分液漏斗及溴水和CCl4能除去NaBr溶液中的少量NaI
③海水提溴与海带提碘均涉及氧化还原反应
④制备粗硅的反应为C+SiO2![]() Si+CO2↑
Si+CO2↑
⑤SiO2与Al2O3均能与强碱溶液反应,所以均为酸性氧化物
⑥光导纤维的成分主要是Si
A.①②③B.②③④
C.②④⑥D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃条件下向10.00 mL 0.1 mol·L-1HCOOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如下图所示(忽略温度变化)。下列说法中不正确的是( )
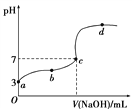
A. a点表示的溶液中c(HCOO-)约为10-3 mol·L-1
B. 用25 mL的酸式滴定管量取HCOOH溶液
C. c点NaOH溶液的体积小于10 mL
D. 在a、c间任一点,溶液中一定都有c(Na+)>c(HCOO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种优良的水处理剂。25℃,其水溶液中加酸或碱改变溶液的pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=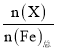 ]。下列说法正确的是( )
]。下列说法正确的是( )

A.K2FeO4、H2FeO4都属于强电解质
B.25℃,H2FeO4+H+![]() H3FeO4+的平衡常数K>100
H3FeO4+的平衡常数K>100
C.由B点数据可知,H2FeO4的第一步电离常数Ka1=4.15×10-4
D.A、C两点对应溶液中水的电离程度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com