
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是![]()
①含有大量![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
②![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]()
③加入Mg能放出![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
④澄清透明溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
⑤中性溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
⑥稀硫酸中:![]() 、
、![]() 、
、![]() 、
、![]()
⑦![]() 溶液中:
溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
⑧![]()
![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
⑨通入大量![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]() 。
。
A.②③④⑧B.②③⑤⑦C.①②③⑨D.④⑤⑥⑨
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】中医认为,明矾[KAl(SO4)2·12H2O]具有解毒杀虫,燥湿止痒,止血止泻,清热消痰的功效。实验室用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制取明矾的流程如下图所示。请回答下列问题:

(1)明矾溶于水后呈________性(填“酸”、“碱”或“中”);其原因是______(用离子程式表示)。
(2)明矾溶于水后所得的溶液中各离子浓度由大到小的顺序是__________。
(3)向明矾溶液中逐滴加Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH_____7(填“>”、“<”、“=”),离子反应总方程式为_________________
(4)为尽量少引入杂质,流程中的“试剂”应选用______________(填标号)。
A.NaCl溶液 B.KOH溶液 C.氨水 D.H2SO4溶液
(5)流程图中“沉淀”的化学式为_________________。
(6)已知:Kw=l.0×10-14,Al(OH)3![]() AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于________________
AlO2-+H++H2O,K=2.0×10-13:则Al(OH)3与NaOH溶液反应的平衡常数等于________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )

A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将n mol·L-1氨水滴入10 mL 1.0 mol·L-1 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是

A. a点KW=1.0×10-14
B. b点:c(NH)>c(Cl-)>c(H+)>c(OH-)
C. 25 ℃时,NH4Cl水解常数为(n-1)×10-7(用n表示)
D. d点水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(g)![]() cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是

A. T1<T2,Q>0
B. 增大压强,B的转化率减小
C. 当反应达平衡时,混合气体的密度不再变化
D. a+b>c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
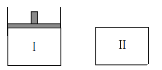
【题目】已知Ⅰ容器恒压,Ⅱ容器恒容,其它条件相同时,在Ⅰ、Ⅱ中分别加入3molZ,起始时容积相同,发生反应2X(g)+2Y(s)![]() 3Z(g)并达平衡。下列说法正确的是
3Z(g)并达平衡。下列说法正确的是
A.从起始到平衡所需时间:Ⅰ>Ⅱ
B.平衡时Z的转化率:Ⅰ<Ⅱ
C.平衡后若在Ⅰ中再加入0.1molY,则X的物质的量将减少
D.平衡后若在Ⅱ中再加入2molZ,则新平衡时Z的体积分数变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中微粒的关系正确的是![]()
A.![]() 时,
时,![]() 的氯化铵溶液中:
的氯化铵溶液中:![]()
B.![]() 时,
时,![]() 的氯化铵溶液中:
的氯化铵溶液中:![]()
C.将![]() 的醋酸溶液稀释后,恢复至原温度,pH和
的醋酸溶液稀释后,恢复至原温度,pH和![]() 均增大
均增大
D.向![]() 溶液中加入等物质的量的NaOH形成的溶液中:
溶液中加入等物质的量的NaOH形成的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法中正确的是![]()

A.图中A、B、D三点处![]() 的大小关系:
的大小关系:![]()
B.若处在B点,将![]() 的硫酸与
的硫酸与![]() 的KOH溶液等体积混合,溶液显中性
的KOH溶液等体积混合,溶液显中性
C.![]() 时,保持温度不变,在水中加入适量
时,保持温度不变,在水中加入适量![]() 固体,体系可从A点变化到C点
固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
B. 食品包装材料聚乙烯因发生加成反应而易老化
C. ![]() 的名称为4—苯基—2—丁醇
的名称为4—苯基—2—丁醇
D. 重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com