
【题目】可逆反应aA(g)+bB(g)![]() cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是

A. T1<T2,Q>0
B. 增大压强,B的转化率减小
C. 当反应达平衡时,混合气体的密度不再变化
D. a+b>c+d
科目:高中化学 来源: 题型:
【题目】含氯消毒剂是消毒剂中常用的一类产品。
I.某实验小组用如图装置制备家用消毒液。
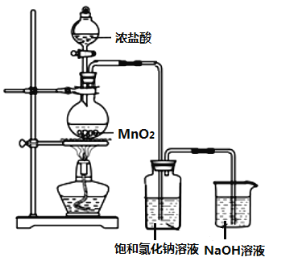
(1)图中盛装浓盐酸的仪器名称是___,写出利用上述装置制备消毒液涉及反应的化学方程式,制氯气:___、制消毒液:___。此方法获得的消毒液的有效成分是___(填名称)。
(2)洗气瓶中饱和食盐水的作用是___。
(3)此消毒液在使用时应注意一些事项,下列说法正确的是___。
a.可以用于衣物消毒
b.可以用于瓷砖、大理石地面的消毒
c.可以用于皮肤消毒
d.与洁厕灵(含盐酸)混合使用效果更好
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol,则被氧化的NH3在标准状况下的体积为___L,该过程中电子转移的总数为___个。
II.(5)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。氯酸钠与盐酸在50℃的条件下反应得到二氧化氯和氯气的混合气体。控制50℃的加热方法是___,写出该反应的化学方程式___。
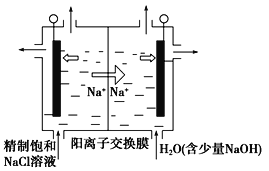
(6)目前已开发出用电解法制取ClO2的新工艺。
如图所示,用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH ⑧H2O2 ⑨NH3 ⑩CO2
(1)既有极性共价键又有非极性共价键的是__(用序号表示)。
(2)既有离子键又有共价键的是__(用序号表示)。
(3)共价化合物有___(用序号表示)。
(4)CO2的电子式___;Na2O2的电子式__。
(5)用电子式表示MgCl2的形成过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水溶液中发生电离:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。下列叙述不正确的是( )
H++A2-。下列叙述不正确的是( )
A. 在NaHA溶液中一定是:c(Na+)>c(HA-)>c(OH-)>c(H+)
B. 在Na2A溶液中一定是:c(Na+)>c(A2-)>c(OH-)>c(H+)
C. 在NaHA溶液中一定是:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. 在H2A溶液中一定是:c(H+)=c(HA-)+2c(A2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 有相同容积的定容密封容器甲和乙,甲中加入
有相同容积的定容密封容器甲和乙,甲中加入![]() 和
和![]() 各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度 B. 甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D. 甲增加0.1mol ![]() ,乙增加0.1mol I2
,乙增加0.1mol I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝电池性能优越,Al-Ag2O2电池用于电解尿素[CO(NH2)2]的碱性溶液制备氢气(隔膜Ⅱ仅阻止气体通过,a、b均为惰性电极)。下列说法正确的是( )
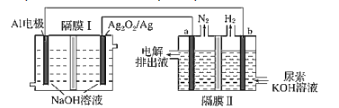
A.Ag电极是正极,反应后该电极区溶液pH减小
B.原电池的总反应为:2Al+3Ag2O2+2NaOH═2NaAlO2+3Ag2O+H2O
C.每消耗2.7g铝,理论上a、b两极共产生气体3.36L(标准状况)
D.a电极上的电极反应为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
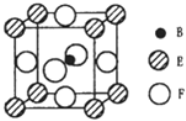
【题目】一种离子晶体的晶胞如图其中阳离子A以红球表示,阴离子B以黑球表示。

(1)每个晶胞中含A离子的数目为___________,含B离子数目为____________。
(2)若A的核外电子排布与Ar相同,B的电子排布与Ne相同,则该离子化合物的化学式是_________;
(3)阳离子周围距离最近的阴离子数为_______,阴离子周围距离最近的阳离子数为________。
(4)已知A的离子半径为rm,则该晶胞的体积是_________m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行如下实验,研究化学反应中的热量变化。

请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________反应(填“放热”或“吸热”,下同),Ba(OH)2·8H2O与NH4Cl的反应是________反应。
(2)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,该反应的中和热为______,表示其中和热的热化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素的原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)F的基态原子价电子排布式为____________________ 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为_______________(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是______________
A 分子中都含有σ键和π键
B 中心原子都sp杂化
C 都是含极性键和非极性键的非极性分子
D 互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+,其原因是BD分子中含有_________
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示.B位于E和F原子紧密堆积所形成的空隙当中.与一个F原子距离最近的F原子的数目为_________,该晶体的化学式为_______.若该晶体的相对分子质量为M,阿伏加德罗常数为NA,B、E、F三种元素的原子半径分别为r1pm、r2pm、r3pm,则该晶体的密度表达式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com