
【题目】强酸与强碱的稀溶液发生中和反应的热效应为H+(aq)+OH(aq)![]() H2O(l) ΔH=57.3 kJ/mol。稀醋酸、浓硫酸、稀硝酸分别与1.0 L 0.1 mol·L1的NaOH溶液恰好完全反应,放出的热量与消耗NaOH溶液的体积之间的关系如图所示(CH3COOH电离要吸热)。则下列描述正确的是
H2O(l) ΔH=57.3 kJ/mol。稀醋酸、浓硫酸、稀硝酸分别与1.0 L 0.1 mol·L1的NaOH溶液恰好完全反应,放出的热量与消耗NaOH溶液的体积之间的关系如图所示(CH3COOH电离要吸热)。则下列描述正确的是
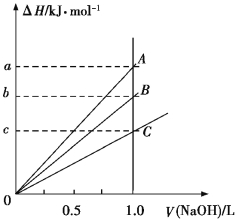
A.A表示稀硝酸与NaOH溶液的反应
B.B表示稀醋酸与NaOH溶液的反应
C.b=5.73
D.C表示浓硫酸与NaOH溶液的反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将0.1 mol铜与40 mL 10 mol/L HNO3充分反应后,溶液中含a mol H+。由此可知
A.生成的气体在标准状况下的体积为4.48 L
B.生成的气体在标准状况下的体积为1.49 L
C.被还原的硝酸的物质的量为(0.2a)mol
D.反应后溶液中所含![]() 的物质的量为0.2 mol
的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁二酮肟(![]() )是检验Ni2+的灵敏试剂。
)是检验Ni2+的灵敏试剂。
(1)Ni2+基态核外电子排布式为________。丁二酮肟分子中C原子轨道杂化类型为________,1 mol丁二酮肟分子所含σ键的数目为________,分子中各原子的电负性由大到小的顺序为________________。
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点-19.3 ℃,沸点42.1 ℃,易溶于有机溶剂。
①Ni(CO)4固态时属于________晶体(填晶体类型)。
②与CO互为等电子体的阴离子为____________(填化学式)。
(3)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应或操作会明显产生吸热现象的是
A. 将氢氧化钠溶液迅速倒入盛有盐酸的量热计中 B. 浓硫酸加水稀释
C. 氯化铵固体和氢氧化钡固体在烧杯中混合搅拌 D. 甲烷的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制SO2并验证SO2某些性质的装置图,试回答:

(1)⑥中发生反应的化学方程式为_____________________________________。
(2)①中实验现象为__________________,证明SO2是________气体。
(3)②中品红溶液_______________,证明SO2有________性。
(4)③中现象是____________________,证明SO2有________性。
(5)④中现象是____________________,证明SO2有________性。
(6)⑤的作用是_____________________,反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前三周期元素A、B、C、D,原子序数依次增大,A的基态原子的L层电子是K层电子的两倍;B的价电子层中的未成对电子有3个;C与B同族;D的最高价含氧酸为酸性最强的无机含氧酸。请回答下列问题:
(1)C的基态原子的电子排布式为_____________;D的最高价含氧酸酸性比其低两价的含氧酸酸性强的原因是___________________________。
(2)杂化轨道分为等性和不等性杂化,不等性杂化时在杂化轨道中有不参加成键的孤电子对的存在。A、B、C都能与D形成中心原子杂化方式为____________的两元共价化合物。其中,属于不等性杂化的是____________(写化学式)。以上不等性杂化的化合物价层电子对立体构型为_________,分子立体构型为_______________________________。
(3)以上不等性杂化化合物成键轨道的夹角________(填“大于”、“等于”或“小于”)等性杂化的化合物成键轨道间的夹角。
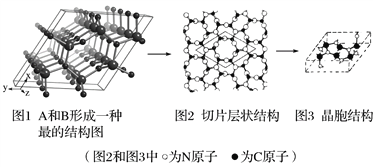
(4)A和B能形成多种结构的晶体。其中一种类似金刚石的结构,硬度比金刚石还大,是一种新型的超硬材料。其结构如下图所示(图1为晶体结构,图2为切片层状结构),其化学式为________________。实验测得此晶体结构属于六方晶系,晶胞结构见图3。已知图示原子都包含在晶胞内,晶胞参数a=0.64 nm,c=0.24 nm。其晶体密度为________________(已知:![]() =1.414,
=1.414,![]() =1.732, 结果精确到小数点后第2位)。
=1.732, 结果精确到小数点后第2位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72 L CH4 ②3.01×1023个HCl ③13.6 g H2S ④0.2 mol NH3,下列对四种气体的关系表示不正确的是
A. 体积④<①<③<② B. 密度①<④<③<②
C. 质量④<①<③<② D. 氢原子数④<②<③<①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com