
【题目】下列各组物质相互反应后,没有碱生成的是 ( )
A.Na2O2溶于水
B.红热的铁和水蒸气
C.金属钠投入水中
D.Na2O投入水中
科目:高中化学 来源: 题型:
【题目】根据下列变化关系,请回答下列问题:(A~E均分别代表一种物质,框图中的部分产物已略去,如A生成D的同时还有CO2生成)
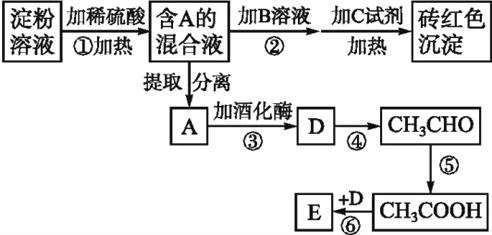
(1)写出A物质的名称____。加B溶液的作用为______________。
(2)写出D的结构简式_________________。
(3)写出下列反应的化学方程式:
③__________________________________。
④__________________________________。
⑥__________________________________。
(4)反应⑥的反应类型是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤造成的污染是大气污染的主要原因,利用下列反应可减少燃煤污染:
SO2(g)+2CO(g) ![]() 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
下列有关该反应的判断正确的是( )
A.使用催化剂改变了反应途径,但ΔH没变
B.升高温度,反应速率加快,反应放出的热量增多
C.反应物的化学计量数之和等于生成物的化学计量数之和,故压强对转化率无影响
D.在容积固定的容器中进行反应时,若混合气体的密度不再改变,则该反应不一定达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中有反应:aX(g)+bY(s)nW(g) ΔH=Q kJ·mol-1。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,做出了如下曲线图:

其中,w(W)表示W在气体混合物中的百分含量,t表示反应时间。其他条件不变时,下列分析正确的是( )
A.图Ⅰ可能是不同压强对反应的影响,且p2>p1,a<n
B.图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好
C.图Ⅱ可能是不同压强对反应的影响,且p1>p2,n=a+b
D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL混合液中,HNO3和H2SO4的物质的量浓度分别为0.4mol/L和0.1mol/L。向该混合液中加入1.92g铜粉,加热使反应发生完全。下列说法正确的是(忽略反应前后溶液体积变化)( )
A.所得溶液中c(Cu2+)=0.225mol/L B.所得溶液中c(Cu2+)=0.03mol/L
C.所得气体在标准状况下的体积为0.448L D.反应中转移0.06mol的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验。
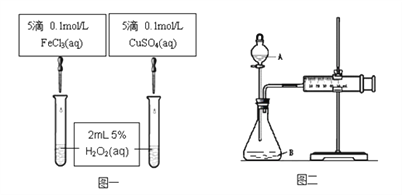
(1) 图一可通过观察____________________现象来定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是__________________,你认为还可以作其他何种改进? _____________________。
(2) 图二可用于定量比较反应的快慢,检查图二装置气密性的方法是________________。
利用图二做实验时需测量的数据是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氮可由NO和O2生成,已知在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)2NO2(g) ΔH,n(NO)、n(O2)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)/mol | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(1)已知:K800 ℃>K1 000 ℃,则该反应的ΔH________0(填“大于”或“小于”),用O2表示0~2 s内该反应的平均速率为________。
(2)能说明该反应已达到平衡状态的是________。
a.容器内气体颜色保持不变
b.2v逆(NO)=v正(O2)
c.容器内压强保持不变
d.容器内气体密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动,应采取的措施有________。
(4)在题述条件下,计算通入2 mol NO和1 mol O2的平衡常数K=________。
(5)在题述条件下,若开始通入的是0.2 mol NO2气体,达到化学平衡时,NO2的转化率为________。
(6)煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
①CH4(g)+4NO(g) ![]() 2N2(g)+CO2(g)+2H2O ΔH<0
2N2(g)+CO2(g)+2H2O ΔH<0
②CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) ΔH<0
N2(g)+CO2(g)+2H2O(g) ΔH<0
对于反应②,欲提高NO2的转化率,可采取的措施有________。
a.增加原催化剂的表面积
b.降低温度
c.减小投料比[n(NO2)/n(CH4)]
d.增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
A. 9.0 B. 9.5 C. 1 0.5 D. 1 1.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述中不正确的是( )
A.0.1molNaCl固体中含0.1NA个阳离子
B.22.4LCO2含有的原子数是3NA
C.常温常压下,NA个H2质量为2g
D.1molMg与足量O2反应,失去的电子数是2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com