
阅读以下内容,回答问题。
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2,或CO)法;③活泼金属置换法;④电解法。四种方法各有优缺点,在工业上均有应用。
(1)一种无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别为________(填序号)。
A.O2、CO2 B.O2、CO
C.CO2、CO D.CO、CO2
(2)下列说法错误的是________(填序号)。
A.对废旧金属最好的处理方法是回收、再利用
B.提炼金属要经过矿石的富集、冶炼、精炼三步
C.活泼金属的冶炼都是通过电解其盐溶液制得
D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
(3)钛(Ti)有“未来钢铁”之称,工业上常以TiCl4 +2Mg
+2Mg Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行________(填序号)。
Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行________(填序号)。
A.稀有气体中 B.空气中
C.氮气中 D.CO2气体中
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
下列对合成材料的认识不正确的是( )
A.有机高分子化合物称为聚合物或高聚物,是因为它们大部分是由小分子通过聚合反应而制得的

D.高分子材料可分为天然高分子材料和合成高分子材料两大类
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四种装置中,均盛200mL的溶液。
①0.005 mol/LCuSO4溶液,②0.01 mol/LH2SO4,③ZnCl2溶液,④KCl溶液.

(1)上述四种装置中,为电解池的是 (用编号回答),装置①中两电极的电极反应式分别是:阴极: ,阳极: ;
(2)若将装置④中的外加电源拆去,用导线将两个电极连接,则Fe极上发生的反应是___________________,C极上发生的反应是 。
(3)工作一段时间后,测得导线上均通过0.002mol电子,则上述装置②中生成气体的体积是________ mL (溶液体积变化忽略不计);
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示为800 ℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是
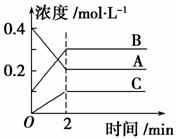
A.发生的反应可表示为:2A(g)  2B(g)+C(g)
2B(g)+C(g)
B.前2 min A的分解速率为0.1 mol·L-1·min-1
C.开始时,正逆反应同时开始
 D.2 min时,A、B、C的浓度之比为2∶3∶1
D.2 min时,A、B、C的浓度之比为2∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列几种关于金属冶炼方法的叙述中,正确的是( )
A.蒸发海水制成饱和食盐水,将其电解可制得金属钠
B.炼铁高炉中,利用焦炭作为还原铁矿石的还原剂
C.高炉炼铁能得到纯铁
D.铝热法能够使氧化铁跟铝在高温条件下炼出铁来
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中溶解和悬浮着大量的无机物和有机物,具有巨大的开发潜力,人类除了从海水中获得食盐和水外,还获得大量的钾、镁、溴、碘等,以下说法正确的是( )
A.从海水中可以得到NaCl,NaCl是制造纯碱的原料
B.海水中含有碘元素,只需将海水中的碘升华就可以得到碘单质
C.电解氯化钾和氯化镁的水溶液,可制得钾和镁
D.用有机溶剂可萃取海水中的溴、碘
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性学习小组在实验室中模拟海水提取溴的过程,其实验流程如下:


 Br2
Br2
(1)取24 L除去悬浮杂质后的海水,浓缩至2 L;
(2)向其中通入足量Cl2,反应的离子方程式:______________,通入热空气的目的:______________________;
(3)将吹出的Br2用纯碱溶液吸收,反应得到NaBr、NaBrO3和CO2,反应的化学方程式:________________________________,产生的CO2通入足量澄清石灰水中,得到1 g 白色沉淀;
(4)将吸收Br2的溶液用足量硫酸处理得到Br2单质,反应的化学方程式:____________________________,理论上可以得到Br2的质量为________;
(5)请计算海水中溴的浓度为________ g/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
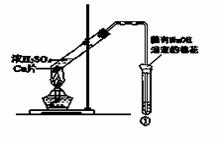
用下图所示装置进行实验,下列对实验现象的解释不合理的是
| ①中试剂 | ①中现象 | 解 释 | |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
做实验时不小心粘了一些高锰酸钾,皮肤上的斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:
MnO4-+C2O42-+H+-→CO2↑+Mn2++ 

关于此反应的叙述正确的是 ( )
A.该反应的氧化剂是C2O42-
B.该反应右边方框内的产物是OH-
C.该反应中生成1molCO2电子转移数总是5NA
D.配平该反应式后,H+的系数是16
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com