
【题目】下列说法正确的是
A.需要加热方能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关试剂的保存方法,错误的是
A. 浓硝酸保存在棕色试剂瓶中并放置在阴凉处
B. 少量的金属钠保存在煤油中
C. 液溴应保存在棕色细口瓶中,并加水液封
D. 新制的氯水通常保存在无色细口瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3,如图。已知该分子中N-N-N 键角都是108.1°,下列有关 N(NO2)3 的说法不正确的是( )

A. 该分子中既含有非极性键又含有极性键
B. 分子中四个氮原子不共平面
C. 该物质既有氧化性又有还原性
D. 15.2g 该物质含有6.02×1022个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全世界每年被腐蚀损耗的钢铁量非常惊人,在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因。
(1)在潮湿空气中,钢铁发生吸氧腐蚀时的正极反应式为________________________。
(2)已知草酸分解的化学方程式为:H2C2O4![]() CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是________________。
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是________________。
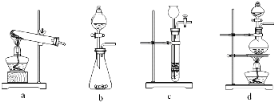
(3)某实验小组利用草酸分解产生的CO和铁锈反应来测定铁锈样品的组成(假定铁锈中只有Fe2O3· nH2O和Fe两种成份),实验装置如下图所示。

①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是_______、________(填答案编号)。
a. 浓硫酸 b.澄清的石灰水 c. 氢氧化钠溶液 d. 无水氯化钙
②在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;(b)____________。
③E装置的作用是___________________________________________________________ 。
④准确称量样品10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =_____________。
⑤在本实验中,下列情况会使测定结果n偏大的是__________(填答案编号)。
a.缺少装置B b.缺少装置E c.反应后的固体中有少量Fe2O3·nH2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在周期表中的相对位置如图所示。W、X、Y、Z原子的最外层电子数之和为21。下列说法中错误的是
![]()
A. 元素X的单质能与强酸、强碱反应
B. W的氢化物水溶液可以用于刻蚀玻璃
C. 气态氢化物的稳定性:W>Y
D. 简单阴离子的还原性:W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请用化学用语回答下列问题:
(1)F在元素周期表中的位置为_______________。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为____________________________________________。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为_________________。写出在空气中长期放置生成H的化学反应方程式为:___________________________________。H的溶液与稀硫酸反应产生的现象为____________________________________。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________________________________。
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为_______________;原NaOH溶液的物质的量浓度为____________;由曲线X、Y可知,两次实验通入的CO2的体积比为_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO![]() 被还原为NO),最终溶液体积为1L。下列说法正确的是( )
被还原为NO),最终溶液体积为1L。下列说法正确的是( )
A. 反应后生成NO的体积为33.6 L (标况)
B. 所得溶液中c(Fe2+)∶c(Fe3+)=1∶2
C. 所得溶液中c(NO![]() )=2.75 mol·L-1
)=2.75 mol·L-1
D. 所得溶液中的溶质只有FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH3COONa溶液存在水解平衡:CH3COO-+H2O![]() CH3COOH+OH-,下列说法正确的是( )
CH3COOH+OH-,下列说法正确的是( )
A. 加入少量固体FeCl3, c(CH3COO-)增大
B. 加入少量NaOH固体,c(CH3COO-)增大
C. 稀释溶液,溶液的pH增大
D. 加入适量醋酸得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镁是一种浅黄色粉末,易水解生成氢氧化镁和氨气,常用于制备其它超硬、高导热、耐高温的氮化物。实验室用以下装置制取干燥、纯净的N2并与金属镁反应制取氮化镁。

已知:Mg + 2NH3![]() Mg(NH2) 2+ H2
Mg(NH2) 2+ H2
回答下列问题:
(1)装置A的分液漏斗中盛装的试剂是________;B、F中盛装碱石灰的仪器名称是_______。
(2)连接好装置进行实验前经检查装置的气密性良好。其他实验步骤如下:
①装药品 ②点燃C处酒精灯 ③点燃E处酒精灯 ④打开A中分液漏斗
正确的先后顺序为_________________(填序号)。
(3)与分液漏斗相连通的橡胶管的作用是_________________________________。
(4)C中反应的化学方程式是_____________________________________________。
(5)D装置的作用是_______________________________________________。
(6)若24.0g镁放入E装置中,实验结束后称得E增加了7.0g,则氮化镁的产率是_________。
(7)设计简单实验证明E中得到的固体中含有氮化镁________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com