
【题目】铬是人体必需的微量元素,铬元素形成的化合物很多,常见的有Cr2O3、(NH4)2Cr2O7、[Cr(CH3COO)2]22H2O等,请回答下列问题:
(1)铬熔点较高,一般应用铝热反应制备铬单质。写出利用Cr2O3制备单质铬的化学方程式 ____________________ 。
(2)实验室常用Fe2+处理含(NH4)2Cr2O7的废水,其流程如下:
Cr2O72﹣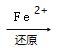 Cr3+
Cr3+![]() Cr(OH)3↓
Cr(OH)3↓
①(NH4)2Cr2O7中铬的化合价为 ________ 。
②第一步的离子方程式为_____ 。
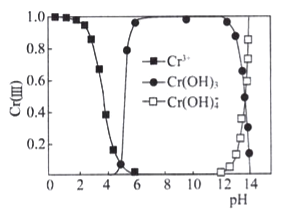
③已知三价铬[Cr(III)]在水溶液中的存在形态随pH的变化如下图,为尽可能除去铬元素实现废水达标排放,pH要控制在_______;若pH过高,溶液中残留铬量增大,其原因是 __________
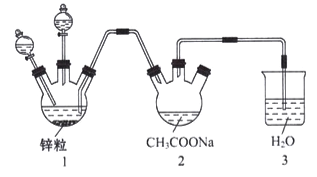
(3)醋酸亚铬水合物{[Cr(CH3COO)2]22H2O,相对分子质量为376} 是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为制备醋酸亚铬水合物,其装置如图所示,且仪器1中预先加入锌粒。
已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
a.Zn+2HCl═ZnCl2+H2↑
b.Zn+2CrCl3═2CrCl2+ZnCl2
c.2Cr2++4CH3COO+2H2O═[Cr(CH3COO)2]22H2O↓
①以上发生的反应中,属于氧化还原反应的是_______(填序号)。
②往仪器1中加入盐酸和三氯化铬溶液的顺序是先加入盐酸一段时间后再加入三氯化铬溶液,然后再加入盐酸。这样做的主要目的是____________________。
③已知其他反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1molL-1实验后得干燥纯净的[Cr(CH3COO)2]22H2O 9.48 g,则该实验所得产品的产率为 __________(保留两位有效数字)。
【答案】2Al+Cr2O3![]() 2Cr+Al2O3+6(价)Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+6~12Cr(OH)3转化为可溶性的Cr(OH)4-ab让锌粒与盐酸先反应产生H2,把装置中的空气赶出,避免生成的亚铬离子被氧化,然后再加入盐酸,利用产生的氢气把液体压入右边的仪器84%
2Cr+Al2O3+6(价)Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+6~12Cr(OH)3转化为可溶性的Cr(OH)4-ab让锌粒与盐酸先反应产生H2,把装置中的空气赶出,避免生成的亚铬离子被氧化,然后再加入盐酸,利用产生的氢气把液体压入右边的仪器84%
【解析】本题考查铬元素及其化合物性质、制备的知识点,可从题给的已知信息和图像及相关基础知识入手,根据氧化还原反应、离子反应、溶液的PH和实验操作的有关知识进行解答。
(1)Al的还原性大于Cr,可发生2Al+Cr2O3![]() 2Cr+Al2O3
2Cr+Al2O3
(2)①根据化合物中,化合价代数和为0,可知 (NH4)2Cr2O7中铬的化合价为+6
②Cr2O72﹣有氧化性,Fe2+有还原性,发生氧化还原反应,第一步的离子方程式为 Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+ 。
③除去铬元素实现废水达标排放,须使铬元素全部生成Cr(OH)3沉淀,由图像可知pH要控制在6~12之间。若pH过高,Cr(OH)3溶解于碱中,生成溶于水的Cr(OH)4- ,溶液中残留铬量增大。
(3)①a、b反应中有元素化合价的改变,是氧化还原反应,c 中元素化合价未变,不是氧化还原反应,因此属于氧化还原反应的是a、c
②二价铬不稳定,易被氧气氧化,为了防止被氧化,首先需要排尽装置中的空气,三氯化铬溶液在2装置中反应,必须将1装置中的三氯化铬溶液压入2中,所答案为:让锌粒与盐酸先反应产生H2,把装置中的空气赶出,避免生成的亚铬离子被氧化,然后再加入盐酸,利用产生的氢气把液体压入右边的仪器
③ CrCl3的物质的量为9.51/158.5=0.06(mol),醋酸钠的物质的量为1.5*0.1=0.15(mol),根据 2CrCl2+4CH3COONa+2H2O═[Cr(CH3COO)2]22H2O↓+4NaCl可知CrCl3全反应,则[Cr(CH3COO)2]22H2O的物质的量为0.03mpl,质量为0.03*376g=11.28g,产率为9.48/11.28=0.84,所以产率为84%。


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐
B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应
D.一元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.将铜丝插入稀硝酸中:Cu+4H++2NO3-![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe![]() 2Fe2+
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O![]() Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下在2L的密闭容器中,充入2mol SO2和1molO2发生反应:2SO2(g) + O2(g) ![]() 2SO3(g)△H=﹣196kJmoL-1,当气体的总物质的量减少0.8mol时反应达到平衡,下列有关叙述不正确的是( )
2SO3(g)△H=﹣196kJmoL-1,当气体的总物质的量减少0.8mol时反应达到平衡,下列有关叙述不正确的是( )
A.保持温度不变,向平衡后的容器中再充入1molSO2和0.5molO2时,V(正)>V(逆)
B.相同温度下,起始时向容器中充入2mol SO3,达平衡时SO3的转化率为20%
C.平衡混合气体中S02的物质的量为1.2mol
D.保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收39.2kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“混盐”是指一种金属离子与多种酸根阴离子构成的盐,如氯化硝酸钙[Ca(NO3)Cl]就是一种混盐。“复盐”是指多种简单阳离子和一种酸根阴离子构成的盐,如:KAl(SO4)2。下列化合物中属于“混盐”的是( )
A. BiONO3 B. (NH4)2Fe(SO4)2 C. Ca(ClO)Cl D. K3Fe(CN)6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
A. 冰醋酸、纯碱、蓝矾、生石灰分别属于酸、碱、盐、氧化物
B. HC1O、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸
C. 漂白粉、冰水、氯水均为混合物
D. Na2O、NaOH、NaCl、Na2SO4、Na2O2都属于钠的含氧化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A. 简单离子半径:W<X<Z B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com