
| A. | 六氟化氙(XeF6) | B. | 次氯酸(HClO) | C. | 三氟化硼(BF3) | D. | 氮气 (N2) |
分析 根据分子中,中心原子的最外层电子数与成键数之和为8,则分子中所有原子都满足最外层8电子结构.
解答 解:A.XeF6中,Xe的最外层多于8个电子,故A错误;
B.HClO中H元素的化合价为+1,H原子核外电子数为1,所以1+1=2,H原子不满足8电子结构,故B错误;
C.BF3中,B位于第ⅢA族,则3+3=6,不满足所有原子都满足最外层8电子结构,故C错误;
D.N2中N原子最外层5个电子,氮气结构式为N≡N,N原子形成3个共价键,每个共价键提供一个电子,所以每个N原子周围电子数为:5+3=8,故D正确;
故选D.
点评 本题考查原子核外电子排布,注意原子的最外层电子数及判断ABn型分子的一般规律来解答,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
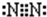 ;乙分子的结构式
;乙分子的结构式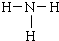 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
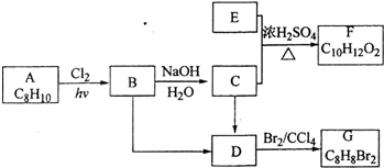

 +H2O
+H2O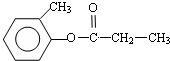 、
、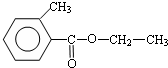
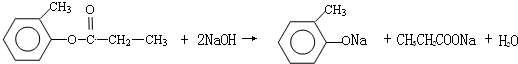 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A. | 该反应的化学方程式是:CO (g)+H2O (g)?CO2 (g)+H2(g) | |
| B. | 上述反应的正反应是放热反应 | |
| C. | 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应为平衡状态 | |
| D. | 某温度下,如果平衡浓度符合下列关系式:$\frac{c(C{O}_{2})}{3c(CO)}$=$\frac{c({H}_{2}O)}{5c({H}_{2})}$,判断此时的温度是1000℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com