
【题目】对于反应C(s)+H2O(g)![]() CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
A.升高温度B.增大水蒸气浓度
C.加入大量CD.降低压强
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】洗煤和选煤过程中排出的煤矸石(主要含Al2O3、SiO2及Fe2O3)会占用大片土地,造成环境污染。某课题组利用煤矸石制备聚合氯化铝流程如下:
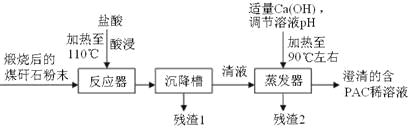
已知:聚合氯化铝([Al2(OH)nCl6-n]m(1≤n≤5,m≤10),商业代号PAC)是一种新型、高效絮凝剂和净水剂。
(1)酸浸的目的是___________________________;实验需要的500mL3.0 mol·L-1的盐酸,配制时所需要的玻璃仪器除量筒、烧杯、玻璃棒外还有______________________。
(2)若m=n=2,则生成PAC的化学方程式是_____________________。
(3)从含PAC的稀溶液中获得PAC固体的实验操作方法是_______、_________、_________。
(4)为了分析残渣2中铁元素的含量,某同学称取5.000g残渣2,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液;然后移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定,消耗标准溶液20.00mL。已知反应式为Fe2++MnO4-+H+—Fe3++Mn2++H2O(未配平)。判断滴定终点的依据是_______________________;残渣2中铁元素的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生做了如下4个实验:
①在铝盐溶液中逐滴加入稀氨水直至过量;
②在明矾溶液中加入氢氧化钡溶液直至过量;
③在含少量氢氧化钠的偏铝酸钠溶液中通入二氧化碳直至过量;
④在少量盐酸的氯化铝溶液中加入氢氧化钠至过量。
在4个图像,纵坐标为沉淀物质的量,横坐标为溶液中加入物质的物质的量,上述实验与图像对应关系正确的是( )
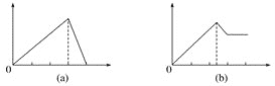
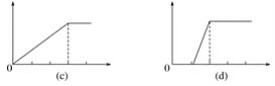
A.①-(d)B.②-(b)C.③-(c)D.④-(a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示有关物质检验的实验结论正确的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀产生 | 该溶液中一定含有SO42- |
B | 向某溶液中加入盐酸,将生成的气体通入品红溶液中,品红溶液褪色 | 该溶液一定含有 SO32- |
C | 将某气体通入品红溶液中,品红溶液褪色 | 说明酸性:H2SO3>H2CO3 |
D | 某气体先通入足量的酸性 KMnO4 溶液,再通入澄清石灰水中有浑浊 | 该气体一定是 CO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应I2(g) + H2(g)![]() 2HI(g) ΔH =-14.9 kJ·mol-1,能说明反应已经达到化学平衡状态的是
2HI(g) ΔH =-14.9 kJ·mol-1,能说明反应已经达到化学平衡状态的是
A.各物质的浓度相等
B.反应容器内压强不变
C.容器内颜色不再变化
D.单位时间内断裂a mol H-H键,同时形成2a mol H-I键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,现有浓度都为0.1mol·L-1HA、HB的溶液各20mL,分别用0.1mol·L-1NaOH溶液滴定。溶液的pH与加入NaOH溶液体积V的关系如图所示。下列判断错误的是
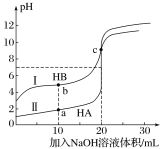
A. 滴定过程中,水电离的c(H+)·c(OH-)均不变
B. 相同条件下,HB的电离程度小于HA的电离程度
C. V=10mL时,c(HB)+c(B-)=2c(Na+)
D. V=20mL时,c(A-)>c(B-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲池是乙醇燃料电池,电解乙池硝酸银溶液。M、N两个电极均为石墨电极,请回答下列问题:
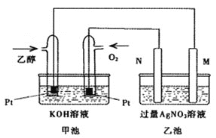
![]() 甲池中乙醇电极名称是______,
甲池中乙醇电极名称是______,![]() 填正极或负极
填正极或负极![]() ,通
,通![]() 的铂电极反应式为_______。一段时间后,该池pH_______
的铂电极反应式为_______。一段时间后,该池pH_______![]() 填增大、减小、不变
填增大、减小、不变![]() 。
。
![]() 乙池中溶液中
乙池中溶液中![]() 的向______极
的向______极![]() 填M或
填M或![]() 移动,在此过程中,乙池中某极析出金属
移动,在此过程中,乙池中某极析出金属![]() 时,甲池中理论上消耗氧气为______
时,甲池中理论上消耗氧气为______![]() 标准状况下
标准状况下![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:
a.![]() ;
;
b.![]()
(1)反应__________(填字母)不能设计成原电池,原因是____________________。
(2)根据上述能设计成原电池的反应,画出简单的原电池实验装置图____________________,并注明电极材料和电解质溶液。写出正极的电极反应式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列有关叙述正确的是( )
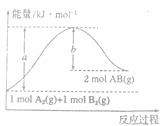
A.每生成2molAB(g)吸收bkJ热量
B.该反应中反应物的总能量高于生成物的总能量
C.反应热ΔH=+(a-b)kJ/mol
D.形成1molA-A键和1mo1B-B键,吸收akJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com