
【题目】某溶液中含有较大量的Cl-、CO32-、OH-,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,正确的操作顺序是
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③
C.①②③②④D.④②③②①
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】光伏发电是当今世界利用太阳能最主要的方式之一。某实验小组提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。如图是该方法的装置示意图(其中电解池中隔膜仅阻止气体通过,阴阳两极均为惰性电极,尿素[CO(NH2)2]中氮元素显-3 价)。
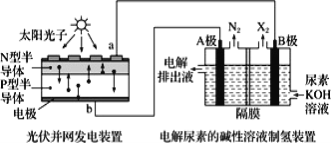
下列叙述正确的是
A.N 型半导体为正极
B.B 极产生的 X2 气体为 O2
C.A 极的电极反应式为 CO(NH2)2-6e-+8OH-=CO32-+N2 ↑+6H2O
D.外电路每转移 0.2 mol 电子,就有 0.2 mol OH-通过隔膜由 A 极区进入 B 极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )
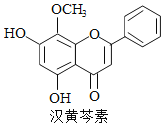
A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液不显色
C. 1 mol该物质与溴水反应,最多消耗2 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.N和Li、Na形成的Li3N、NaN3等化合物具有重要的用途。完成下列填空:
(1)氮原子核外能量最高的电子所处的轨道是:____________。锂离子核外电子的轨道表示式是:____________。
(2)已知Li3N熔点为845℃,NH3熔点﹣77.7℃,用物质结构的知识说明这两种含氮化合物熔点差异的可能原因____________。
II.研究者发明了利用锂循环合成氨的工艺,其流程如下:
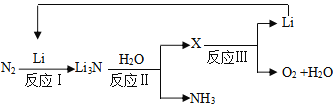
(3)每合成1mol氨,转移电子____________mol;该过程最终得到的氧化产物是____________。
(4)写出反应Ⅱ的化学反应方程式:____________。向0.35gLi3N中加入40mL1mol/L的盐酸,所得溶液中离子浓度由大到小的顺序是:____________。
(5)由元素周期律能得到____________(填序号)。
A.碱性:LiOH<NaOH B.与水反应的剧烈程度:Li<Na
C.溶解度:LiOH<NaOH D.密度:Li<Na
(6)NaN3可用于汽车安全气囊,冲撞时发生如下反应:□NaN3+□KNO3→□K2O+□Na2O+□N2↑,配平此反应的化学方程式,并标出电子转移的数目和方向。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向下列溶液中加入足量Na2O2后,仍能共存的离子是
A.K+、AlO2-、SO42-、Cl-B.Na+、Cl-、CO32-、SO32-
C.Ca2+、Mg2+、HCO3-、NO3-D.NH4+、Ba2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉)。请回答:
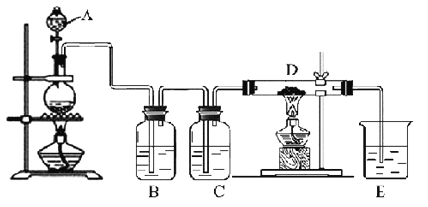
(1)仪器A的名称是________,烧瓶中反应的化学方程式是_____________________。
(2)装置B中盛放液体是___,气体通过装置B的目的是__________________,装置C中盛放的液体是_________。
(3)D中反应的化学方程式是__________________________________________。
(4)烧杯E中盛放的液体是_____,反应的离子方程式是___________。
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应.为收集D中产物,在D与E之间,除增加收集装置外,还需要增加__装置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,所给离子一定能大量共存的是
A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.小苏打溶液:K+、SO42-、Cl-、H+
C.与铝反应产生H2的溶液中:Na+、K+、CO32-、Cl-
D.室温下,强酸性溶液中:Na+、Fe3+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
(2)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。
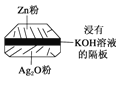
根据上述反应式,完成下列题目。
(1)下列叙述正确的是________。
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:___________________________________________________________。
(3)使用时,负极区的pH________(填“增大”“减小”或“不变”,下同),正极区的pH______,电解质溶液的pH________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com