
125 53 |
125 53 |


科目:高中化学 来源: 题型:
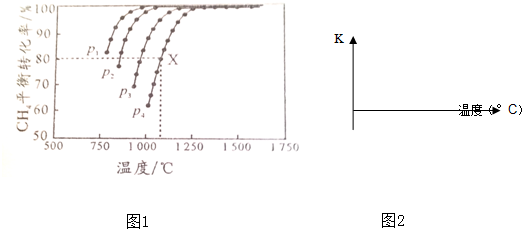 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
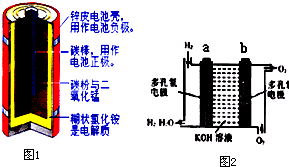
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
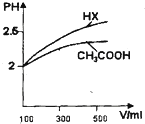 已知25℃时部分弱电解质的电离平衡常数数据如下表
已知25℃时部分弱电解质的电离平衡常数数据如下表| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | Ka1=4.3×10-7、Ka2=5.6×10-11 |
| H2SO3 | Ka1=1.0×10-2、Ka2=1.02×10-7 |
| c(H2SO3) |
| c(HSO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
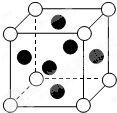 【物质结构与性质】
【物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | D | E | F | G |
| 所有原子中半径最小 | 基态原子核外只有三个能级,且各能级电子数相等 | 由D形成的两种单质,其中之一是地球生物的“保护伞” | 短周期中第一电离能量小 | 单质为淡黄色晶体,不溶于水,微溶于酒精 | 最外层只有一个电子,次外层填满电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入的NaOH 不够 |
| B、加入的CuSO4 不够 |
| C、未用水浴加热 |
| D、加入的乙醛太少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com