
【题目】工业上以食盐、氨气、二氧化碳等物质为原料制取纯碱。
(1)实验室提纯粗盐的一个重要环节是除去粗盐水中的杂质阳离子。某粗盐样品(主要含Ca2+、Mg2+),提纯该粗盐时,可考虑在粗盐水中加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A____________________、B____________________。
(2)上述实验操作依次为:取样、__________、沉淀、__________、加入盐酸调pH、__________、冷却结晶。
(3)以上“加入盐酸调pH”目的是____________________。
(4)写成工业上以食盐、氨气、二氧化碳等物质为原料制取纯碱反应的化学方程式:
____________________,____________________
(5)氨气与二氧化碳通入的先后顺序是:__________________,因为:____________________。该过程没有析出碳酸钠晶体,其原因是____________________。
(6)标准状况下,吸收11.2升二氧化碳气体,理论上至少需要1mol/L的氨水体积为__________mL。
【答案】 Ca(OH)2或CaO Na2CO3 溶解 过滤 蒸发 将溶液中的碳酸钠和氢氧化钠全部转化为氯化钠 NaCl+NH3+H2O+CO2→NaHCO3↓+NH4Cl 2NaHCO3![]() Na2CO3+H2O+CO2↑ 先通入氨气后通入二氧化碳 氨气的溶解度较大,且生成的氨水呈碱性,有利于二氧化碳的吸收 碳酸钠的溶解度比碳酸氢钠大 500
Na2CO3+H2O+CO2↑ 先通入氨气后通入二氧化碳 氨气的溶解度较大,且生成的氨水呈碱性,有利于二氧化碳的吸收 碳酸钠的溶解度比碳酸氢钠大 500
【解析】 (1). 要除去粗盐水中的杂质阳离子Ca2+、Mg2+,可在粗盐水中加入沉淀剂Ca(OH)2或CaO(CaO与水反应生成Ca(OH)2,所以实际起作用的还是Ca(OH)2。) 将镁离子转化为氢氧化镁沉淀、加入Na2CO3将钙离子转化为碳酸钙沉淀,所以A 为Ca(OH)2或CaO 、B为 Na2CO3 。
(2). 上述实验操作依次为:取样、溶解 、沉淀、过滤 、加入盐酸调pH、蒸发 、冷却结晶。
(3). 以上“加入盐酸调pH”目的是将溶液中的碳酸钠和氢氧化钠全部转化为氯化钠。
(4). 工业上以食盐、氨气、二氧化碳等物质为原料制取纯碱反应的化学方程式:NaCl+NH3+H2O+CO2→NaHCO3↓+NH4Cl,2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(5). 氨气与二氧化碳通入的先后顺序是:先通入氨气后通入二氧化碳 ,因为氨气的溶解度较大,且生成的氨水呈碱性,有利于二氧化碳的吸收 。该过程没有析出碳酸钠晶体,其原因是碳酸钠的溶解度比碳酸氢钠大 。
(6). 标准状况下, 11.2L二氧化碳气体的物质的量为0.5mol,要完全吸收这些气体理论上至少需要氨水0.5mol,所以理论上至少需要1mol/L的氨水体积为500 mL。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,错误的是
A.胶体的本质特征是其分散质粒子直径为1-100nm
B.胶体是胶状的纯净化合物
C.利用丁达尔效应可区分溶液和胶体
D.将饱和FeCl3溶液滴入沸水中,再煮沸可形成红褐色的胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca(OH)2的饱和溶液中存在平衡:Ca(OH)2(s) ![]() Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
A. 升高温度,平衡正向移动
B. 向溶液中加入少量碳酸钠粉末能增大钙离子浓度
C. 恒温下向溶液中加入CaO,溶液的pH不变
D. 向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种有机合成中间体,某研究小组采用如下路线合成X和一种常见的高分子化合物D。首先合成D和乙醇,路线如下:
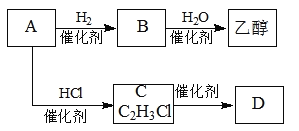
(1)已知A是一种常见的气态烃。写成A分子的结构式____________,C→D的化学方程式是______________,该反应的类型是:_______________。
(2)写出化合物B的结构简式_______________,实验制取B反应的化学方程式_______________。乙醇中官能团的名称是_________。
进一步合成X线路如下:
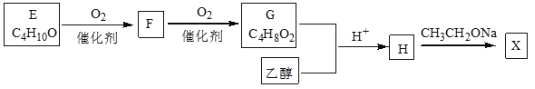
已知:①化合物E的结构中有2个甲基
②![]()
(3)写出H→X的化学方程式是_________________,反应类型是____________________。
(4)若G中混有F,请用化学方法检验F的存在(要求写出简要操作、实验现象和结论)____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯(CH2=CH—CH3)是一种重要的基本化工原料。结合以下合成路线,回答下列问题。
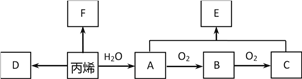
(1)丙烯中所含官能团的名称是_____。
(2)工业上常利用丙烯和氯化氢的反应来制备F,该反应的反应类型是_____。
(3)以丙烯为原料合成有机高分子化合物D。
丙烯→D的化学方程式是_____。
(4)已知:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
以丙烯为原料可以合成一种有香味的物质E。实验室可通过右图所示装置来实现。
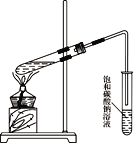
①A→B的化学方程式是:_____。
②A+C→E的化学方程式是:_____。
③若要把制得的E分离出来,应采用的实验操作是_____(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的晶体中,化学键种类相同,晶体类型也相同的是
A.MgO和BaO2 B.SO2和SiO2 C.KOH和NH4Cl D.CCl4和KCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com