
【题目】下列实验操作错误的是
A.用蒸馏的方法分离汽油和煤油
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.浓硫酸稀释时,应将浓硫酸慢慢加到水中,及时搅拌并冷却
D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
科目:高中化学 来源: 题型:
【题目】下图是实验室制备四氯化硅液体的装置。已知:四氯化硅熔点为-70℃,沸点57.6℃,遇水极易反应。

请回答下列问题。
(1)写出装置A中发生反应的离子方程式_______________________________。
(2)8.7 g MnO2 和足量的浓盐酸反应,其中被氧化的HCl的物质的量为____________mol。
(3)装置B中盛放的试剂是__________________;
(4)g管的作用是_________________。
(5)装置E中冰水的作用是_________________。
(6)干燥管F中碱石灰的作用是______________和_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.次氯酸滴在大理石上不会有气泡产生
B.次氯酸显酸性,所以有杀菌漂白作用
C.用自来水养金鱼时,需将水先晒一段时间,然后注入鱼缸中
D.次氯酸与过氧化钠的漂白原理较相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知下列两个反应:①Fe+H2SO4(稀)=FeSO4+H2![]() ;②Cu+2H2SO4(浓)=CuSO4+SO2
;②Cu+2H2SO4(浓)=CuSO4+SO2![]() +2H2O。试回答下列问题:
+2H2O。试回答下列问题:
(1)反应①中_______元素被还原,反应②中_______元素被还原.(填元素符号)
(2)当反应①生成2gH2时,消耗H2SO4的质量是_______克。
(3)反应②中生成32gSO2气体时,转移_______mol电子。
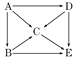
(4)图中表示A~E五种物质的转化关系.若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源.试推断A~E各物质(写化学式):
A_________;B_________;C_________;D_________;E__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体.
(2)基态Fe原子有个未成对电子,Fe3+的电子排布式为 , 可用硫氰化钾检验Fe3+ , 形成的配合物的颜色为 .
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O,乙醛中碳原子的杂化轨道类型为;1mol乙醛分子中含有的σ键的数目为 , 乙酸的沸点明显高于乙醛,其主要原因是 . Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有个铜原子.
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 , 列式表示Al单质的密度gcm﹣3(不必计算出结果).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的二氯取代产物的同分异构体数目分别是( ) 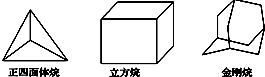
A.2种,4种,8种
B.2种,4种,6种
C.1种,3种,6种
D.1种,3种,8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少大气污染,许多城市推广汽车使用清洁燃料.目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG).这两类燃料的主要成份都是( )
A.碳水化合物
B.碳氢化合物
C.氢气
D.醇类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取Al可采用如图所示工艺流程:
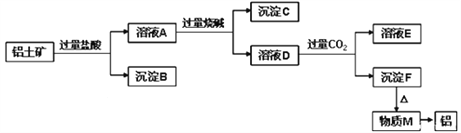
请回答下列问题:
(1)铝土矿加入盐酸后生成Al3+的离子方程式为_____________________________。
(2)沉淀B与烧碱反应的离子方程式为______________________________________。
(3)溶液D中通入过量CO2的离子方程式为_____________________________。
(4)“通入过量CO2”能否改用过量盐酸________(填“能或否”),原因是_____________。
(5)向共含有0.05mol Al3+、Fe3+的溶液中滴入1mol/L NaOH 溶液,生成沉淀的量与加入NaOH 溶液的体积关系如图所示。 则溶液中Al3+的物质的量为_________mol。
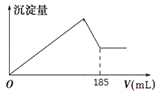
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质混合后,没有离子反应发生的是( )
A. Na2CO3溶液与稀盐酸 B. CuSO4溶液与BaCl2溶液
C. H2SO4溶液与NaCl溶液 D. 稀HNO3与Ba(OH)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com