
【题目】向某溶液中滴加盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。则该溶液一定有
A. CO32-B. NO3-C. SO32-D. SO42-
科目:高中化学 来源: 题型:
【题目】某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是( )
A. 氧化性:ClO->I2>SO42—
B. 蓝色消失的原因是Na2SO3溶液具有漂白性
C. 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝
D. 若将Na2SO3溶液加入氯水中,氯水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面的排序不正确的是
A. 酸性由大到小:HPO3>H3PO4>H3PO3 B. 硬度由大到小:金刚石>碳化硅>晶体硅
C. 熔点由高到低:Na>Mg>Al D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物是日常生活生产中应用广泛的材料。请回答下列问题:
(1)基态铁原子的价电子轨道表达式为_____________________ 。
(2)铁元素常见的离子有Fe2+和Fe3+,稳定性Fe2+____Fe3+(填“大于”“”或“小于”),原因是______________________ 。
(3)纳米氧化铁能催化火箭推进剂NH4ClO4的分解,NH4+的结构式为_________________(标出配位键),空间构型为_______________,其中氮原子的杂化方式为_______________;与ClO4-互为等电子体的分子或离子有______(任写一种)。
(4)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该氧化物中Fe2+、Fe3+、O3-的个数比为___________(填最简整数比)。
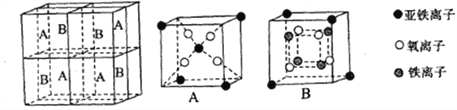
(5)铁有δ、γ、α三种同素异形体,如下图所示。

γ-Fe晶体的一个晶胞中所含有的铁原子数为________,δ-Fe、α-Fe两种晶胞中铁原子的配位数之比为_________。
已知δ-Fe晶体的密度为dg/cm3,NA表示阿伏伽德罗常数的数值,则Fe原子半径为_______Pm(列表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A. 60g丙醇中存在的共价键总数为10NA
B. 1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C. 钠在空气中燃烧可生成多种氧化物。23g钠充分燃烧时转移电子数为1NA
D. 235g核互U![]() 发生裂变反应:
发生裂变反应:![]() +
+![]() n
n![]()
![]() +
+![]() +10
+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、IV四步中对于溶液和沉淀的分离采取的方法是_________;获得沉淀后,要对沉淀进行洗涤,请简述洗涤沉淀的操作是______________________________________。
(2)根据上述框图反应关系,写出下列B、E所含物质的化学式并回答相关问题:
固体B_______;溶液液E_______;沉淀D的重要用途是__________________;KAl(SO4)2的重要用途是_____________________________。
(3)写出写出①、②、③三个反应的离子方程式:①______;②______;③______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com