
【题目】消除氮氧化物和硫氧化物有多种方法。
(1)用活性炭还原法: 某研究小组向某密闭容器中加入足量的活性炭和 NO,发生反应:C(s)+2NO(g) ![]() N2(g)+CO2(g) H=Q kJ·mol-1 在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
N2(g)+CO2(g) H=Q kJ·mol-1 在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:

①0~10 min 内, N2 的平均反应速率 υ(N2)=________ , T1℃时,该反应的平衡常数 K=_____。
②30 min 后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是____________ (填字母)
a. 加入一定量的活性炭 b. 改变反应体系的温度
c. 缩小容器的体积 d. 通入一定量的 NO
③若 30 min 后升高温度至 T2℃,重新达到平衡时,容器中 NO、 N2、 CO2 的浓度之比为 7∶3∶3,则该反应的H______0(填“>” 、 “ =” 、或“<” )
(2)NH3 催化还原法: 原理如图所示
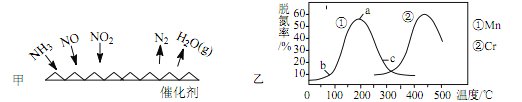
①若烟气中 c(NO2): c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移 1.5mol 电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为_____ 。
②图乙是在一定时间内,使用不同催化剂 Mn 和 Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为_____ ;使用 Mn 作催化剂时,脱氮率 b~a 段呈现如图变化的可能原因是_____。
(3)已知常温下 Ka1(H2SO3)=1.810-2, Ka2(H2SO3)=6.010-9。 汽车尾气中的 SO2 用石灰水来吸收,生成的 CaSO3 浊液 pH=9.0,忽略 SO32-的第二步水解,则Ksp(CaSO3)=_____。
【答案】 0.03 mol·L-1·min-1 K=4 c d < 2NH3(g)+NO(g)+NO2(g) ![]() 2N2(g)+3H2O(g) ΔH=-455.2 kJ/mol Mn 、200℃ b~a段,温度较低,催化剂活性较低,脱氮反应速率较慢,反应还没达到化学平衡(反应限度),随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致脱氮率逐渐升高; 4.2×10-9
2N2(g)+3H2O(g) ΔH=-455.2 kJ/mol Mn 、200℃ b~a段,温度较低,催化剂活性较低,脱氮反应速率较慢,反应还没达到化学平衡(反应限度),随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致脱氮率逐渐升高; 4.2×10-9
【解析】(1)①分析图表数据结合化学反应速率概念计算v,计算平衡浓度结合平衡常数概念是生成物浓度的幂次方乘积除以反应物的幂次方乘积得到;②反应前后是气体体积不变的反应,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大,说明改变的条件是缩小体积增大浓度,或加入一氧化氮达到新平衡后个物质浓度增大;③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为7:3:3,根据Qc与K的相对大小判断平衡移动方向,逆反应方向是吸热反应,正反应为放热反应;
(2)①得电子化合价降低的反应物是氧化剂;
②
(3)
(1)①分析图表数据,0~10min内,N2的平均反应速率v(N2)=0.03 mol/(L/min),
化学平衡三段式列式计算平衡浓度:
C(s)+2NO(g)= N2(g)+CO2(g);
起始量(mol/L) 1 0 0
变化量(mol/L) 0.8 0.4 0.4
平衡量(mol/L) 0.2 0.4 0.4
K=![]() =4
=4
②30min后,只改变某一条件,反应重新达到平衡,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大;a.加入一定量的活性炭是固体,对平衡无影响,故a不符合;
b.改变反应体系的温度, 达到平衡后一氧化氮、氮气、二氧化碳浓度不可能都增大,故b不符合;c.当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故c符合;d.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,适故答案为:bc;
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为7:3:3,Qc=![]() <4,,这说明升高温度平衡向逆反应方向移动,因此逆反应是吸热反应,则正反应是放热反应,故Q<0,故答案为:<;
<4,,这说明升高温度平衡向逆反应方向移动,因此逆反应是吸热反应,则正反应是放热反应,故Q<0,故答案为:<;
(2)①由图甲可知NH3与NO、NO2反应产物为N2和水,故氧化剂为NO、NO2;因此反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-455.2 kJ/mol;
②根据图乙知Mn催化剂时,在200℃左右脱氮率最高,Cr作催化剂,500℃左右脱氮率最高,但二者的最高脱氮率差不多,使用Mn作催化剂需要的温度低,更经济,因此使用的最佳的催化剂和相应的温度分别为Mn、200℃左右;故答案为:Mn、200℃;使用 Mn 作催化剂时,脱氮率 b~a 段呈现上升状态,可能的原因是:b~a段,温度较低,催化剂活性较低,脱氮反应速率较慢,反应还没达到化学平衡(反应限度),随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致脱氮率逐渐升高;
(3)由Ka2(H2SO3)=6.0×10-9可知SO32-+H2OHSO3-+OH-的水解Kh=![]() ==1.67×10-6,
==1.67×10-6,
常温下,测得某纯CaSO3与水形成的浊液pH为9,c(HSO3-)=c(OH-)=1×10-5,可知c(SO32-)=![]() =6×10-5,
=6×10-5,
又c(Ca2+)=c(SO32-)+c(HSO3-)=7×10-5,
Ksp(CaSO3)=c(Ca2+)×c(SO32-)=7×10-5×6×10-5=4.2×10-9。


科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒擦入1 L 1 molL﹣1食盐水中.下列说法正确的是( ) 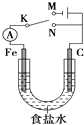
A.若电键K与N连接,铁被保护不会腐蚀
B.若电键K与N连接,正极反应式是4OH﹣﹣4e﹣=2H2O+O2↑
C.若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D.若电键K与M连接,当两极共产生28 L(标准状况)体时,生成了1 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒温、恒容的密闭容器中进行下列两个可逆反应:(甲)2X(g)![]() Y(g)+Z(s); (乙)A(s)+2B(g)
Y(g)+Z(s); (乙)A(s)+2B(g)![]() C(g)+D(g),当下列物理量不再发生变化时,可以表明甲和乙均达到平衡状态的是
C(g)+D(g),当下列物理量不再发生变化时,可以表明甲和乙均达到平衡状态的是
①混合气体密度
②反应容器中生成物的百分含量
③反应物的消耗速率与生成物的消耗速率之比等于化学计量数之比
④混合气体的压强
⑤固体质量
⑥混合气体的总物质的量
A.①②③④⑤⑥ B.①②③⑤ C.①②③ D.②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们日常生活中出现了“加碘食盐”、“增铁酱油”、“富硒茶叶”和“含氟牙膏”等商品。这里的碘、铁、硒、氟应理解为( )
A.元素B.单质C.分子D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小组利用下列装置检验草酸亚铁晶体受热分解的部分产物。
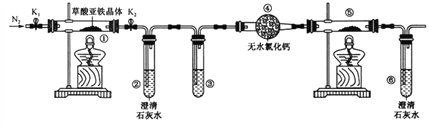
下列说法正确的是
A. 若③和⑤中分别盛放足量NaOH溶液和CuO,可检验生成的CO
B. 实验时只需要在装置①中反应结束后再通入N2
C. 若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气
D. 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属硼的合金及其化合物有着广泛的用途。
(1)硼钢合金的硬度是普通钢材的 4 倍,其主要成分是铁。 画出基态铁原子的价电子排布图_____。
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键, 则氨硼烷分子结构式为_____。写出一种与氨硼烷互为等电子体的分子_____(填化学式)。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如右图所示。
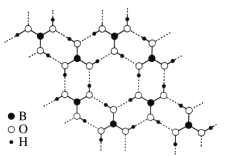
①1 mol H3BO3晶体中含有______mol 氢键。
②请从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:__________。
(4)硼氢化钠是一种常用的还原剂。其晶胞结构如右图所示:

①该晶体中Na+的配位数为_____。
②H3BO3 分子中的 O—B—O 的键角_____(填“大于”、“等于”或“小于”) BH4-中的 H—B—H 的键角,判断依据是_____。
③已知硼氢化钠晶体的密度为 ρ g/cm3, NA代表阿伏伽德罗常数的值,则 a=_____(用含 ρ、 NA的代数式表示);④若硼氢化钠晶胞上下底心处的 Na+被 Li+取代,得到的晶体的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达正确的是
A. Na2O2的电子式:![]()
B. Al3+的结构示意图:![]()
C. CH3COOCH3的名称:乙酸甲酯
D. 用电子式表示氯化氢的形成过程:![]() +
+![]() →
→![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车在我国正迅猛发展,磷酸铁锂(LiFePO4)电池是电动汽车常用的一种电池,其工作原理如下图所示。中间是聚合物的隔膜把正极与负极隔开,锂离子可以通过而电子不能通过。该电池的总反应式是:LiFePO4+C6 ![]() Li1-xFePO4+LixC6 。下列说法不正确的是
Li1-xFePO4+LixC6 。下列说法不正确的是
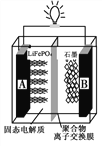
A. 放电时电子从A极通过导线流向B极
B. 充电时Li+从A极区移向B极区
C. 充电时B极电极反应式为:C6+xLi++xe-===LixC6
D. 放电时A极电极反应式为:Li1-xFePO4+xLi++ xe-=== LiFePO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类对原子结构的认识经历了一个不断深入的过程,以下科学家以及他们提出的原子结构学说(或模型)对应关系正确的是 ( )
A.道尔顿——电子轨道理论B.卢瑟福——量子力学模型
C.玻尔——行星绕太阳模型D.汤姆逊——葡萄干面包模型
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com