
����Ŀ��[���ʽṹ������]
����NaOH��Cu(OH)2����Һ�����ڼ���ȩ����Ҳ�����ں������Ƿ�Ӧ�Ʊ�����Cu2O��
��1��Cu+��̬��������Ų�ʽΪ
��2����OH����Ϊ�ȵ������һ�ַ���Ϊ ���ѧʽ����
��3��ȩ����̼ԭ�ӵĹ���ӻ������� ��1mol��ȩ�����к������ļ�����ĿΪ ��
��4������NaOH��Cu(OH)2����Һ����ȩ��Ӧ�Ļ�ѧ����ʽΪ ��
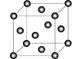
��5��Cu2O��ϡ����������Cu��CuSO4��ͭ�����ṹ��ͼ��ʾ��ͭ������ÿ��ͭԭ����Χ���������ͭԭ����ĿΪ ��
���𰸡���1��[Ar]3d10
��2�� HF
��3�� sp2 6mol
��4�� CH3CHO+NaOH+2Cu(OH)2![]() ��H3COONa+Cu2O��+3H2O
��H3COONa+Cu2O��+3H2O
��5�� 12
��������
���⣨1��Cuλ�ڵ������ڵ�IB�壬29��Ԫ�أ�Cu��ʧȥ�����1�����ӣ���������Ų�ʽΪ��Ar��3d10��1s22s22p63s23p63d10����2���ȵ����壺ԭ��������ȣ��۵�������Ҳ��ͬ������OH����2��ԭ�ӡ�8�����ӣ����õ�һ�����ӱ��9�����ӣ�����FԪ�أ���HF����3����ȩ��̼ԭ����3���������µ��Ӷԣ��۲���Ӷ���Ϊ3���ӻ���������ڼ۲���Ӷ��������ӻ�����Ϊsp2����ȩ�Ľṹ��ʽCH3CHO�����ɼ�Ԫ��ֻ���γ�1��������������ȩ�к���6mol������6��6.02��1023������4��ȩ�������������������������䷴Ӧ����ʽΪ��CH3CHO��2Cu(OH��2��NaOH![]() CH3COONa��Cu2O����3H2O����5��ͭ�ľ������������������ܶѻ�������λ��Ϊ12����ÿ��ͭԭ����Χ���������ͭԭ����Ϊ12��
CH3COONa��Cu2O����3H2O����5��ͭ�ľ������������������ܶѻ�������λ��Ϊ12����ÿ��ͭԭ����Χ���������ͭԭ����Ϊ12��


 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ģ���������Ƽ����ȡNaHCO3�IJ���װ�á����в�����ȷ����( )

A. aͨ��CO2��Ȼ��bͨ��NH3��c�зż�ʯ��
B. bͨ��NH3��Ȼ��aͨ��CO2��c�зż�ʯ��
C. aͨ��NH3��Ȼ��bͨ��CO2��c�з�պϡ�������֬��
D. bͨ��CO2��Ȼ��aͨ��NH3��c�з�պϡ�������֬��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д��ȷ���ǣ� ��
A. ��������NaOH����Һ�м��ȣ�CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr
CH3CH2CH2OH+NaBr
B. ��������Һ��ͨ������������̼��2![]() +CO2+H2O
+CO2+H2O![]()
![]() +Na2CO3
+Na2CO3
C. CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O��+3H2O
CH3COONa+Cu2O��+3H2O
D. CH3COOH + CH3CH218OH![]() CH3COOCH2CH3+H218O
CH3COOCH2CH3+H218O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ͼ��ʾװ�õ���Ȼ�ͭ��Һ��ʵ���й۲쵽̼��I���缫�������ӣ�̼��II���缫������ų�������˵����ȷ����
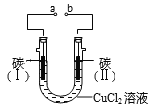
A. aΪ��Դ����
B. �缫���Ϸ�����ԭ��Ӧ
C. ��������a����������b
D. ��װ�ý�����ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��b��![]() ����d��
����d��![]() ����p��
����p��![]() �ķ���ʽ��ΪC6H6������˵����ȷ����
�ķ���ʽ��ΪC6H6������˵����ȷ����
A. b��ͬ���칹��ֻ��d��p����B. b��d��p�Ķ��ȴ����ֻ������
C. b��d��p���������Ը��������Һ��ӦD. b��d��p��ֻ��b������ԭ�Ӵ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ǵ�ƹ�ҵ�ز����ٵĻ���ԭ�ϡ��Ӳ���ַ���(��Ҫ��Fe 42.35%��Cr 9.67%��Ni 5.1%��C 4.7%��Si 3.39%��)����ȡ����������Ĺ����������£�

��֪����Cr3+�백ˮ��Ӧʱ������Cr3+����[Cr(NH3)6]3+��������ʱ��������ֽ⡣Ni2+�백ˮ��Ӧ����[Ni(NH3)6]2+������������ʱ�ȶ����������ữʱ������Ӧ�������Ρ�
��Na2CrO4��Һ�м������pHΪ3.5ʱ��CrO42��ת��ΪCr2O72����
����������ڲ�ͬ�¶�ʱ�ܽ�����±���
�¶��ܽ��/g���� | 20�� | 30�� | 40�� | 60�� | 80�� | 90�� |
Na2SO4 | 19.5 | 40.8 | 48.8 | 45.3 | 43.7 | 42.7 |
Na2Cr2O7 | 183 | 198 | 215 | 269 | 376 | 405 |
(1)���������õ�����Һ����Ҫ����FeSO4��NiSO4��Cr2(SO4)3������NiSO4�Ļ�ѧ����ʽΪ_____���������ʱ������¶�Ϊ90�����ң����Բ��õļ��ȷ�ʽ��_____��
(2)��������ǰ���ʵ����ȵ�Ŀ����_____��
(3)�������������õ���������ϴ�ӣ�����������ϴ�Ӹɾ��ķ�����_____��
(4)��������ʱ�����������������Ʊ�Na2Cr2O7���塣
���������������Na2CO3����ڿ�������������Na2CrO4��CO2���˷�Ӧ�Ļ�ѧ����ʽΪ_____��
���벹�������������պ������Ʊ�Na2Cr2O7����(�Ⱥ�ɫ)��ʵ�鷽����ˮ�������ˣ�_____����Na2Cr2O7����(����ʹ�õ��Լ��У����ᣬ����ˮ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 18g����(��ND2)�к��еĵ�����Ϊ10NA
B. һ��������������22.4L(��״��)Cl2�ڹ��������·���ȡ����Ӧ���γ�C��Cl������ĿΪ2NA
C. �ö��Ե缫���100mL0.1mol��L��1��CuSO4��Һ��������������������ͬ�����µ����������ʱ����·��ת�Ƶ�����Ϊ0.04NA
D. n(H2SO3)��n(HSO3��)֮��Ϊ1mol��KHSO3��Һ�У����е�K+��ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����δ��Ǵ�������ҩ�����е�һ����Ȼ����ϳɵ��δ��IJ���·�����£�
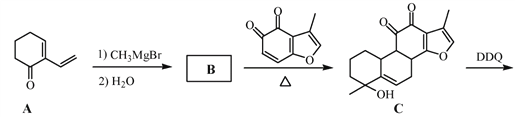
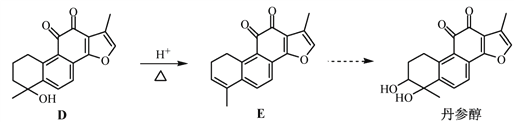
��֪��![]()
��1��A�еĹ���������Ϊ__________________��д���֣���
��2��D![]() E�ķ�Ӧ����Ϊ__________________��
E�ķ�Ӧ����Ϊ__________________��
��3��B�ķ���ʽΪC9H14O��д��B�Ľṹ��ʽ��__________________��
��4��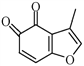 ��һ��ͬ���칹��ͬʱ��������������д����ͬ���칹��Ľṹ��ʽ��_________��
��һ��ͬ���칹��ͬʱ��������������д����ͬ���칹��Ľṹ��ʽ��_________��
�ٷ����к��б���������FeCl3��Һ������ɫ��Ӧ�����ܷ���������Ӧ��
�ڼ�������ˮ���������ֲ���ữ������о�ֻ��2�ֲ�ͬ��ѧ�������⡣
��5�����![]() ��
��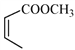 Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ�����Լ����Ҵ����ã��ϳ�·������ͼʾ����������ɣ���
�ĺϳ�·������ͼ�����Լ����Ҵ����ã��ϳ�·������ͼʾ����������ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��W��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ(�������P��Ӧ��������ȥ����Ӧ������ˮ��Һ�н���)![]() ��A
��A![]() B
B![]() C��
C��
����AΪ�д̼�����ζ�����壬ˮ��Һ�ʼ��ԣ�CΪ����ɫ���壬��ˮ��Ӧ����һԪǿ��D��D����ǿ�����ԡ�
(1)�ڴ��������£�A��C��Ӧ��������������Ⱦ���ʣ��÷�Ӧ��ѧ����ʽΪ_______��
(2)��ҵ�ϳ��ù�����Na2CO3��Һ����C�����ɵ����ʵ��������������Σ��÷�Ӧ�����ӷ���ʽΪ___��
����A��C��W���dz������壬C�ǵ����������Ҫ���壬������A��C��Ӧ����B����÷�Ӧ�Ļ�ѧ����ʽΪ_____��
ij��ѧ�С�齫�Ѽ�����һ���������걣�����ܱ������У�ÿ��һ��ʱ��������pH����������ʼһ��ʱ���ڣ������pH�ʼ�С���ƣ������ӷ���ʽ����ԭ��________��
��A��B��C�������ʵ���Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��C����������ķ��ݼ������ȷֽ������B��������״����2.24L��Wͨ��150mL1 molL-1 ��A��Һ�У���ַ�Ӧ���ܷ�Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com