
【题目】将50g溶质质量分数为w1,物质的量浓度为c1的浓硫酸沿玻璃棒加入到Vml水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀溶液.下列说法中正确的是( )
A. 若c1=2c2,则w1<2w2,V<50 mL
B. 若c1=2c2,则w1<2w2,V>50 mL
C. 若w1=2w2,则c1<2c2,V=50 mL
D. 若w1=2w2,则c1>2c2,V<50 mL
【答案】A
【解析】试题分析:A、B、设物质的量是浓度为c1molL﹣1的密度为ρ1,物质的量是浓度为c2molL﹣1硫酸溶液的密度为ρ2,利用c=![]() 公式变形计算硫酸的质量分数,结合硫酸溶液的浓度越大密度越大,进行判断;
公式变形计算硫酸的质量分数,结合硫酸溶液的浓度越大密度越大,进行判断;
稀释前后溶质的质量不变,结合质量分数关系,判断稀释后溶液的质量小于100g,故水的质量小于50g,据此判断水的体积;
C、D、根据稀释前后溶质的质量不变计算混合后溶液的质量为100g,计算水的质量为50g,据此计算水的体积;
设物质的量是浓度为c1molL﹣1的密度为ρ1,物质的量是浓度为c2molL﹣1硫酸溶液的密度为ρ2,利用c=![]() 计算硫酸的浓度,结合浓硫酸溶液的浓度越大密度越大,进行判断.
计算硫酸的浓度,结合浓硫酸溶液的浓度越大密度越大,进行判断.
解:A、若c1=2c2,设物质的量是浓度为c1molL﹣1的密度为ρ1,物质的量是浓度为c2molL﹣1硫酸溶液的密度为ρ2,则:ω1=![]() ,ω2=
,ω2=![]() ,所以
,所以![]() =
=![]() =
=![]() ,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故ω1<2ω2,稀释前后溶质的质量不变,所以稀释后溶液的质量小于100g,故水的质量小于50g,水的密度为1g/ml,所以水的体积V<50ml;故A正确;
,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故ω1<2ω2,稀释前后溶质的质量不变,所以稀释后溶液的质量小于100g,故水的质量小于50g,水的密度为1g/ml,所以水的体积V<50ml;故A正确;
B、由A分析可知,所以水的体积V<50ml,ω1<2ω2,故B错误;
C、稀释前后溶质的质量不变,若ω1=2ω2,则稀释后溶液的质量为100g,所以水的质量为50g,水的密度为1g/ml,所以水的体积V=50ml;设物质的量是浓度为c1molL﹣1的密度为ρ1,物质的量是浓度为c2molL﹣1硫酸溶液的密度为ρ2,则:c1=![]() ,c2=
,c2=![]() ,所以
,所以![]() =
=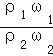 =
=![]() ,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故c1>2c2,故C错误;
,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故c1>2c2,故C错误;
D、由C中分析可知,水的体积V=50ml,c1>2c2,故D错误.故选:A.


科目:高中化学 来源: 题型:
【题目】氢能是一种高效洁净的新能源,用氢作能源的燃料电池汽车备受青睐。氢能具有的优点包括( )
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①②B.①③C.②④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。以下有关分析正确的选项是
A.熔融状态下该晶体能导电B.K3C60中碳元素显-3价
C.K3C60中只有离子键D.C60与12C互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将40℃时的饱和KCl溶液冷却至10℃,该过程中保持不变的是
A. KCl的溶解度 B. 溶剂的质量 C. 溶质的质量分数 D. 溶液中K+的数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B═C+D,8g A和12g B恰好完全反应,生成C和9g D,则生成C的质量为( )
A. 9g B. 10g C. 11g D. 12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数的叙述正确的是:
A. 17g OH-含有9×6.02×1023个电子
B. 12.4g白磷中含有磷原子数为0.4NA
C. 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
D. 标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com