
【题目】在自来水生产过程中,不涉及化学变化的是
A.杀菌消毒B.调节水的pH
C.过滤水中的泥沙D.沉淀水中的Ca2+和Mg2+
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①NaHCO3溶液加水稀释,![]() 的比值保持增大
的比值保持增大
②浓度均为0.1molL-1的Na2CO3、NaHCO3等体积混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1molL-1氨水中滴加0.1molL-1盐酸,恰好完全中和时pH=a,则由水电离产生的c(OH-)=10-amolL-1
④已知:Ksp(AgCl)=1.8×l0-10,Ksp(Ag2Cr2O4)=2.0×l0-12,则Ag2CrO4的溶解度小于AgCl
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列达到平衡状态的标志是( )
4NO(g)+6H2O(g),下列达到平衡状态的标志是( )
A. 达到化学平衡时5v正(NH3)=4v逆(O2)
B. 单位时间内生成4 mol NO的同时,消耗4 mol NH3
C. NH3、O2、NO、H2O的物质的量之比满足4∶5∶4∶6
D. 恒温恒容,气体的密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )

A. C元素是非金属性最强的元素
B. A元素最高价氧化物对应的水化物具有强氧化性
C. B元素的氧化物、氢化物的水溶液都呈酸性
D. 三种元素的原子半径的大小顺序是:B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。下列方框中对应的物质或有关叙述正确的是( )
![]()
A. Na2S4O6、H2O、Na2S2O3、Au2O、NaOH B. Na2S2O3、NaOH、Na2S4O6、Au2O、H2O
C. Na2S2O3、H2O、Na2S4O6、Au2O、NaOH D. 当1 mol Au2O3完全反应时,转移电子8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )

A. Na+、Fe3+、K+、ClO—都可在该物质的溶液中大量共存
B. 该物质可以用于氧化还原滴定测定K2Cr2O7含量
C. 向0.1mol/L该物质的溶液中逐滴滴加0.1mol/LNaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如右图所示
D. 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42—完全沉淀的离子方程式为:Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)为紫黑色粉末,是一种新型高效消毒剂。K2FeO4易溶于水,微溶于浓KOH溶液,在0 ℃~5 ℃的强碱性溶液中较稳定。一般制备方法是先用Cl2与KOH溶液在20 ℃以下反应生成KClO(在较高温度下则生成KClO3),KClO再与KOH、Fe(NO3)3溶液反应即可制得K2FeO4。实验装置如图所示:
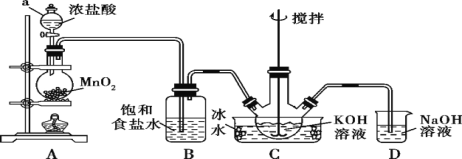
回答下列问题:
(1)制备KClO。
①仪器a的名称是________________;装置B吸收的气体是________。
②装置C中三颈烧瓶置于冰水浴中的目的是______________;装置D的作用是_____________。
(2)制备K2FeO4。
①装置C中得到足量KClO后,将三颈烧瓶上的导管取下,加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度,搅拌,当溶液变为紫红色,该反应的离子方程式为________________________________。
②向装置C中加入饱和________溶液,析出紫黑色晶体,过滤。
(3)测定K2FeO4纯度。测定K2FeO4的纯度可用滴定法,滴定时有关反应的离子方程式为:
a.FeO42-+CrO2-+2H2O═CrO42-+Fe(OH)3↓+OH-
b.2CrO42-+2H+═Cr2O72-+H2O
c.Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
称取2.0g制备的K2FeO4样品溶于适量KOH溶液中,加入足量的KCrO2,充分反应后过滤,滤液在250mL容量瓶中定容.取25.00mL加入稀硫酸酸化,用0.10 molL-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液的体积为24.00mL,则该K2FeO4样品的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀H2SO4 和稀HNO3的混合液1L,其物质的量浓度分别为0.4mol·L-1和0.1mol·L-1。若向该混合液中加入足量的铜粉,则最多能溶解铜粉的质量为( )
A. 2.4gB. 3.2gC. 6.4gD. 9.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按单质、氧化物、酸、碱分类顺序排列,其中正确的是
A. 氧气、干冰、硫酸、烧碱 B. 碘酒、冰、盐酸、烧碱
C. 氢气、二氧化硫、硝酸、纯碱 D. 铜、硫酸钠、醋酸、石灰水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com