


 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ö����ЧӦ���� |
| B�����ǵ���� |
| C����NaOH��Һ����FeCl3��Һ���к��ɫ�������ɣ�����Fe��OH��3������û�г��� |
| D�����ù��˵ķ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol Cl2�μӷ�Ӧת�Ƶĵ�����ΪNA |
| B����0�棬101kPaʱ��22.4L�����к���2NA����ԭ�� |
| C��1molO2������Ϊ32g/mol |
| D��2molHCl�ܽ���1Lˮ�еõ�������Һ�����ʵ���Ũ��Ϊ2mol/l |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ��� �� | ���� | ���� |
| A | ������CO2ͨ��CaCl2��Һ�� | �ް�ɫ ���� | ����Ca��HCO3��2����ˮ |
| B | �����½�AlƬ����Ũ������ѧ���� | ���������� | AlƬ��Ũ�����Ӧ |
| C | �ò�����պȡŨ��ˮ�㵽��ѧ����ɫʯ����ֽ�� | ��ֽ����ɫ | Ũ��ˮ�ʼ��� |
| D | ��SO2ͨ����ˮ�� | ��Һ��ɫ | SO2����Ư ���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
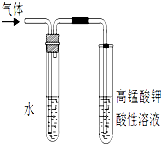 �������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ���
�������ڲ�ͬ�ܼ�����NaOH������ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com