
| y |
| 4 |
 ,以此判断.
,以此判断.| 12 |
| 4 |
 ,
, ;
; ,烃A可能有的结构简式为:(CH3)3CCH=CH2、(CH3)2C=C(CH3)2、CH2=C(CH3)CH(CH3)2等,
,烃A可能有的结构简式为:(CH3)3CCH=CH2、(CH3)2C=C(CH3)2、CH2=C(CH3)CH(CH3)2等,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
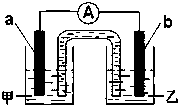 一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-=2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu═2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e-═Cu2+,还原反应式:2Fe3++2e-=2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将40 g NaOH溶解在1 L水中 |
| B、将22.4 L HCl气体溶于水配成1 L溶液 |
| C、将1 L 10 mol/L浓盐酸加入9 L水中 |
| D、将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com