
【题目】M是石油裂解气的重要成分,由M制备环酯P的合成路线(部分反应条件略去)如图所示:

已知在特殊催化剂的作用下,能够发生碳碳双键两边基团互换的反应,如:
2CH2=CHR![]() CH2=CH2+RCH=CHR
CH2=CH2+RCH=CHR
回答下列问题:
(1)M的名称是____________,A中的含氧官能团名称是____________。
(2)①的反应类型是___________,⑥的反应类型是________________。
(3)C的结构简式为____________。由C→G的过程中步骤④、⑥的目的是___________。
(4)G中最多有_______个原子共平面,其顺式结构式为_____________。
(5)符合下列条件D的同分异构体有______种。
①氯原子连在碳链的端点碳上 ②羟基连在不同的碳原子上,其中核磁共振氢谱为4组峰且峰面积比为4:2:2:1的为__________(写结构简式)。
(6)由I和G在一定条件下制取环酯P的化学方程式为_________________。
(7)已知:  根据题中信息,设计以2-氯丙烷制备环己烯的合成路线(无机试剂和溶剂任选)___________。
根据题中信息,设计以2-氯丙烷制备环己烯的合成路线(无机试剂和溶剂任选)___________。
【答案】丙烯 碳碳双键 取代反应 消去反应 HOCH2-CH=CH-CH2OH 保护分子中碳碳双键不被氧化 12 ![]() 10 ClCH2-CH(CH2OH)2
10 ClCH2-CH(CH2OH)2 ![]() CH3-CHCl-CH3
CH3-CHCl-CH3![]() CH2=CH-CH3
CH2=CH-CH3![]() CH2=CH2、CH3-CH=CH-CH3
CH2=CH2、CH3-CH=CH-CH3![]() CH3-CHBr-CHBr-CH3
CH3-CHBr-CHBr-CH3![]() CH2=CH-CH=CH2
CH2=CH-CH=CH2![]()
【解析】
由题中信息可知,M与氯气发生取代反应生成CH2=CH-CH2Cl,可确定M为丙烯;已知在特殊催化剂的作用下,能够发生碳碳双键两边基团互换的反应,则CH2=CH-CH2Cl在催化剂的作用下,生成乙烯、CH2Cl-CH=CH-CH2Cl;根据合成路线可知,A水解后先与HCl发生反应,然后发生氧化反应、消去反应,则A为CH2Cl-CH=CH-CH2Cl、B为乙烯;C为HOCH2-CH=CH-CH2OH;D为HOCH2-CH2-CHCl-CH2OH;E为HOOC-CH2-CHCl-COOH;F为NaOOC-CH=CH-COONa;G为HOOC-CH=CH-COOH;H为CH2Br-CH2Br;I为CH2OH-CH2OH;
(1)根据分析可知,M为丙烯;A为CH2Cl-CH=CH-CH2Cl,含有的官能团为碳碳双键;
(2)反应①为取代反应;反应⑥为卤代烃的消去反应;
(3)C的结构简式为HOCH2-CH=CH-CH2OH,其分子中含有碳碳双键和羟基,这丙种官能团均易发生氧化反应,因此,C→G的过程步骤④、⑥的目的是:为了保护碳碳双键在发生氧化反应时不被氧化;
(4)G的结构简式为HOOC-CH=CH-COOH,当碳碳双键与羧基中碳氧双键确定的平面重合时,则有12原子共平面;其顺式结构为:![]() ;
;
(5)D的结构简式为HOCH2-CH2-CHCl-CH2OH,符合①氯原子连在碳链的端点碳上 ②羟基连在不同的碳原子上。若无支链,固定Cl原子和一个—OH在一端,![]() ,另一个—OH的位置有3种;移动—OH的位置,
,另一个—OH的位置有3种;移动—OH的位置,![]() ,另一个—OH的位置有2种;依此类推,
,另一个—OH的位置有2种;依此类推,![]() ,1种;若存在一个甲基支链,
,1种;若存在一个甲基支链,![]() ,有2种;
,有2种;![]() ,有1种,
,有1种,![]() ,1种,合计10种;其中核磁共振氢谱为4组峰且峰面积比为4
,1种,合计10种;其中核磁共振氢谱为4组峰且峰面积比为4
(6) I、G分别为:HOOC-CH=CH-COOH、CH2OH-CH2OH,在一定条件下发生酯化反应,制取环酯P,其方程式为:![]() ;
;
(7)根据题目信息,烯烃在一定条件下碳碳双键两边的基团可以互换,则先用2-氯丙烷发生消去反应生成丙烯,丙烯在一定条件下生成乙烯和2-丁烯,利用2-丁烯和溴水发生加成反应,生成2,3-二溴丁烷,再发生消去反应生成1,3-丁二烯,最后与乙烯发生双烯合成制取环己烯。合成路线如下:CH3-CHCl-CH3![]() CH2=CH-CH3
CH2=CH-CH3![]() CH2=CH2、CH3-CH=CH-CH3
CH2=CH2、CH3-CH=CH-CH3![]() CH3-CHBr-CHBr-CH3
CH3-CHBr-CHBr-CH3![]() CH2=CH-CH=CH2
CH2=CH-CH=CH2![]()
 。
。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的定容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )

A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.反应进行到10s后停止反应
C.反应开始时10s,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
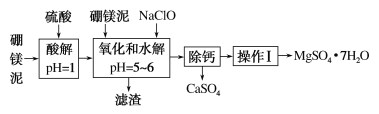
根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸800 mL,若用18.4 mol·L-1的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为________。
A 10 mL B 20 mL C 50 mL D 100 mL
(2)加入的NaClO可将Mn2+氧化为MnO2,反应的离子方程式为:___________________,还有一种离子也会被NaClO氧化,反应的离子方程式为______________________。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外还有_______________。
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:____________________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 |
S(MgSO4)/g | 30.9 | 33.4 | 35.6 | 36.9 |
S(CaSO4)/g | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4的混合溶液中的CaSO4除去,根据上表数据,可确定操作步骤为蒸发结晶、________________(填操作名称)。
(6)实验中提供的硼镁泥共10 g,得到MgSO4·7H2O共17.22 g,则MgSO4·7H2O的产率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液中还可能存在Al3+、Fe2+、NH4+、Ba2+、Cl-、CO32-、SO42-、NO3-中的若干种,现取适量溶液进行如下一系列实验
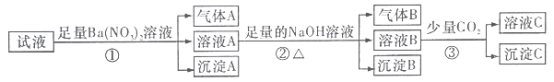
下列有关判断正确的是( )
A. 原试液中一定有Fe2+、SO42-、H+、NH4+、Al3+
B. 原试液中一定没有Ba2+、CO32-、NO3-
C. 步骤③中发生反应的离子方程式为: 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. 沉淀B在空气中由白色迅速变成灰绿色,最终变为红褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家意外发现一种罕见无机化合物YZX2W3(结构如图所示) ,其中W、X、Y为同一短周期元素, X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是

A.元素非金属性强弱顺序为X>Y> W
B.Z的氧化物的水化物是强酸
C.NaY的水溶液不能存放在玻璃试剂瓶中
D.X与Z具有相同的最高化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑。腐蚀原理如右图所示,下列说法正确的是

A. 腐蚀过程中,负极是C
B. Fe失去电子经电解质溶液转移给C
C. 正极的电极反应式为4OH―-4e-==2H2O+O2↑
D. 每生成1mol铁锈(Fe2O3·xH2O)理论上消耗标准状况下的O233.6L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所给的实验装置,下列有关实验的相关叙述正确的是
选项 | 实验装置 | 相关叙述 |
A |
| 实验室可以用该装置和药品制取氨气 |
B |
| 反应过程中,温度降低,Ba(OH)2·8H2O与NH4Cl反应是吸热反应 |
C |
| ①中反应比②中快,说明温度升高可以加快反应速率 |
D |
| 只有氨气等极易溶于水的气体才能利用该装置形成喷泉 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】15.3 g Mg-Al合金(无其他成分),加入到500 mL稀硝酸中,恰好完全反应后,共收集到标准状况下的NO气体11.2 L,向所得溶液中加入4 mol/L NaOH溶液400 mL,得到白色沉淀。下列叙述中正确的是
A.合金中,m(Mg):m(Al)=1:1
B.原稀硝酸的物质的量浓度与NaOH溶液相同
C.白色沉淀的成分为Mg(OH)2
D.过滤后,向白色沉淀中加入原稀硝酸250 mL,可将沉淀全部溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】李比希是 19 世纪最著名和最有成果的化学家。他的贡献之一就是发明了燃烧法测定有机物化学组成。
Ⅰ.某物质完全燃烧后生成二氧化碳和水,现取 3.0g 该物质利用李比希法进行组成测定,无水氯化钙增重 1.8g,浓氢氧化钾溶液增重 4.4g,则该物质的最简式为_________________;
Ⅱ.多种物质符合此最简式,若要确定具体的物质,还需辅助其它的测量手段。
(1)若物质 A 的质谱图如图所示:
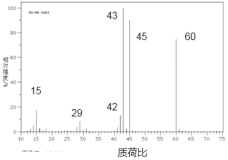
①则 A 的相对分子质量为_____________________;
②若将 A 加入到紫色石蕊试液中变红,则 A 的结构简式为________________;
(2)若测定物质 B 的蒸气密度是相同状况下 H2 的 45 倍
①则 B 的分子式为__________________;
②测定 B 的红外光谱图有 C=O 键、O—H 键、不对称—CH2—等的振动吸收峰,其核磁共振氢谱如图所示,B 的结构简式为_________________;

③取一定量的B物质平均分成2份,一份与足量的NaHCO3作用,一份与足量的Na作用,则产生的CO2与H2的体积比为___;
(3)若测定 C 物质的相对分子质量为 180,且 C 为淀粉水解的最终产物,并且在一定条件下, C 能与上述的 A 物质发生如下转化关系:

①请写出 D 变成 E 的化学方程式___________________;
②已知 G 物质为 D 物质的同系物,相对分子质量比 D 大 14,且其核磁共振H谱显示 3 组峰,面积比为 6:1:1,请写出 G 与 A 发生酯化反应的方程式____________,
Ⅲ.分别将等质量的上述A、B、C三种物质与足量的氧气反应,它们实际消耗氧气的物质的量之比为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com