
【题目】(1)碱洗铝材除其表面的氧化膜,碱洗时常有气泡冒出,原因是____(用离子方程式表示)。为将碱洗后溶液中的铝以沉淀形式回收,最好应加入下列试剂中的________(填字母)。
a.稀H2SO4b.盐酸 c.CO2d.氨水 e.NaOH
(2)已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
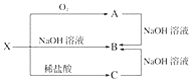
①写出下列物质的化学式:X:___,A:____,B:___,C:_____。
②写出以下反应的离子方程式:A→B:_______;C→B:__________。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ c Al Al2O3 NaAlO2 AlCl3 Al2O3+2OH-=2AlO2-+H2O Al3++4OH-= AlO2-+2H2O
【解析】
(1)Al单质可以和碱反应生成氢气;偏铝酸盐中通入二氧化碳会生成沉淀,且沉淀不会溶解;
(2)X是某金属单质,X、A、B、C含同一种元素,由转化关系可知,X与NaOH反应,且A与NaOH反应,则X为Al,A为Al2O3,B为NaAlO2,C为AlCl3,然后结合物质的性质及化学用语来解答。
(1)Al单质可以和碱反应生成氢气,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;碱洗后Al元素主要以偏铝酸根的形式存在,加入盐酸和硫酸等强酸会先生成沉淀,当酸过量后沉淀会溶解,碱不和偏铝酸盐反应,故选用二氧化碳,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;c;
(2)①X是某金属单质,X、A、B、C含同一种元素,由转化关系可知,X与NaOH反应,且A与NaOH反应,则X为Al,A为Al2O3,B为NaAlO2,C为AlCl3,
故答案为:Al;Al2O3;NaAlO2;AlCl3;
②A为Al2O3,与强碱溶液反应生成偏铝酸盐和水,故答案为:Al2O3+2OH-=2AlO2-+H2O;
C为AlCl3,与过量氢氧化钠反应生成偏铝酸盐和水,故答案为:Al3++4OH-= AlO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】如图为铜与稀硝酸反应的有关性质实验(洗耳球:一种橡胶为材质的工具仪器,可挤压)。
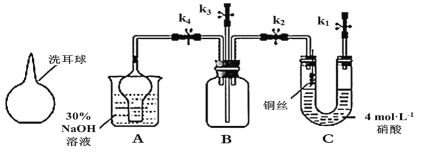
实验步骤如下:
①按照如图装置连接好仪器,关闭所有止水夹。检查装置的气密性。
②在装置A中的烧杯中加入30%的氢氧化钠溶液。在装置C的U型管中加入4.0mol·L-1的硝酸,排除U型管左端管内空气。
③塞紧连接铜丝的胶塞,打开止水夹K1,反应进行一段时间。
④进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色。气体进入烧杯中与氢氧化钠溶液反应。
回答下列问题:
(1)装置C中发生反应的离子方程式为__。反应后的溶液呈蓝色,其原因是铜离子和水分子形成了水合铜离子,1mol水合铜离子中含有σ键数目为12NA,该水合铜离子的化学式为__。
(2)装置A上面的导管口末端也可以连接__来代替干燥管,实现同样作用。
(3)加入稀硝酸,排除U型管左端管内空气的操作是__。
(4)步骤④中“使装置C中产生的气体进入装置B的广口瓶中”的操作是打开止水夹__(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)步骤④中使“气体进入烧杯中与氢氧化钠溶液反应”的操作是__,尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为有__。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为
![]()
实验步骤如下:
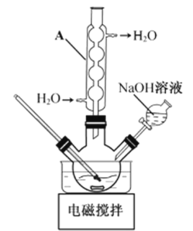
步骤1:如图所示装置的反应瓶中,加入40g氯乙酸、50mL水,搅拌。逐步加入40%NaOH溶液,在95℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是___________;逐步加入NaOH溶液的目的是____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)有以下几种物质:①碳酸氢钠晶体 ②液态氯化氢 ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰 ⑧石墨。试回答(填序号):
(1)以上物质能导电的是_________________________。
(2)以上物质中属于非电解质的是_________________________。
(3)以上物质中溶于水后水溶液能导电的是_________________________。
(4)①、②在水溶液中反应的离子方程式为_________________________________。
(二)某溶液的溶质可能由下列离子组成:Cl-、![]() 、
、![]() 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:
Ⅰ 向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ 向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ 将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
(5)依据以上实验可以推断,原溶液中一定含有____________ (用离子符号表示,下同);一定没有______________;可能含有________________,检验是否存在该离子的方法为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O]是一复盐,在造纸等方面应用广泛。某兴趣小组采用10.0g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾的实验方案如下:
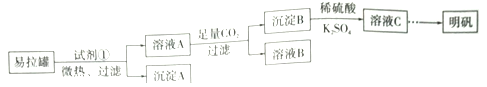
(1)试剂①应选用_____________(填代号)。
a.盐酸 b.H2SO4溶液 c.氯化钠溶液 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为____________________。
(3)溶液B中溶质的主要成分为____________________ (填化学式)。
(4)从溶液C中得到明矾的实验操作步骤为蒸发浓缩、__________(填操作名称)、过滤、洗涤、干燥。如下图所示,蒸发操作中的一处错误是_____________。

(5)该小组在实验完成之后,得到118.5 g明矾,则明矾的回收率为_____________。(已知:明矾的摩尔质量为474g·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是制造LED的重要材料,被誉为“第三代半导体材料”。镓(31Ga)的氧化物和氢氧化物均为两性化合物,工业制备氮化镓的工艺流程如图所示。下列判断正确的是
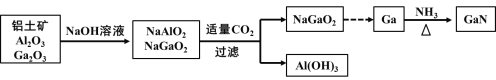
A.Ga位于第五周期第IIIA族B.酸性:Al(OH)3>Ga(OH)3
C.Ga(OH)3可与NaOH反应生成NaGaO2D.Ga与NH3反应的另一种生成物可用作航天燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图像如下:

分析图像,以下结论错误的是( )
A. 析氢腐蚀和吸氧腐蚀的速率一样快
B. 在酸性溶液中生铁可能发生吸氧腐蚀
C. 溶液pH≤2时,生铁发生析氢腐蚀
D. 两溶液中负极反应均为Fe – 2e- = Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜是重要的无机杀菌剂,是一种绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ.模拟制备碱式氯化铜。向CuCl2溶液中通入NH3和HCl,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。
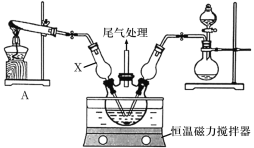
(1)仪器X的名称是______,其主要作用有导气、______。
(2)实验室利用装置A制NH3,发生反应的化学方程式为_______。
(3)反应过程中,在三颈烧瓶内除观察到溶液蓝绿色褪去,还可能观察到的现象有_____。
(4)若体系中NH3过量会导致碱式氯化铜的产量___(填“偏高”、“偏低”或“无影响”),原因为___。
Ⅱ.无水碱式氯化铜组成的测定。称取产品4.29 g,加硝酸溶解,并加水定容至200 mL,得到待测液。
(5)铜的测定:取20.00 mL待测液,经测定Cu2+浓度为0.2 mol·L-1。则称取的样品中 n(Cu2+)=_____mol。
(6)采用沉淀滴定法测定氯:用NH4SCN标准溶液滴定过量的AgNO3(已知:AgSCN是一种难溶于水的白色固体),实验如下图:

①滴定时,应选用下列哪种物质作为指示剂_____(填标号)。
a.FeSO4 b.Fe(NO3)3 c.FeCl3
②重复实验操作三次,消耗NH4SCN溶液的体积平均为10.00 mL。则称取的样品中n(Cl-)=_____mol。
(7)根据上述实验结果可推知无水碱式氯化铜的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
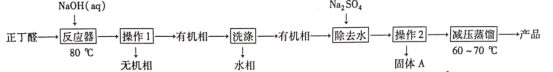
【题目】辛烯醛是重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。
[制备实验]
已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO![]()
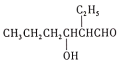
![]()
![]()
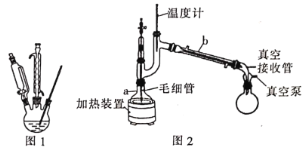
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是___________;使用冷凝管的目的是____________。
(2)操作1中使用的主要仪器名称是___________,有机相从___________(填“上”或“下”)口取出。
(3)判断有机相已洗涤至中性的操作方法:___________。
(4)操作2的名称是_____________;固体A的摩尔质量为322 g·mol-1,固体A的化学式为___________。
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是___________。(填选项)
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是________。(填选项)
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com