
【题目】下列有关Cl2的说法中,不正确的是
A. Cl2是一种黄绿色的有毒气体 B. 干燥的Cl2可保存在钢瓶中
C. 铁丝在Cl2中燃烧生成FeCl3 D. 氯气和液氯是两种不同的物质
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质与条件已略去)。A、C、E、G是中学化学中常见的单质;通常状况下,E是密度最小的气体,G是黄绿色的气体,B是常见的无色液体,F是强碱且焰色反应火焰呈黄色,D是某种具有磁性的金属矿物的主要成分,K受热分解可生成红棕色固体。
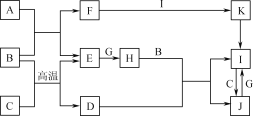
请回答下列问题:
(1) D的化学式为____________。
(2) F的电子式为____________。
(3) 写出J溶液中滴入稀硝酸反应的离子方程式:________________________。
(4) 写出常温下G与F的溶液反应的化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的分类或变化正确的是( )
①混合物:氯水、氨水、水玻璃、水银、食醋、淀粉 ②含有氧元素的化合物叫氧化物 ③CO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2 为碱性氧化物 ④同素异形体:C60、C70、金刚石、石墨 ⑤在熔融状态下能导电的化合物为离子化合物 ⑥强电解质溶液的导电能力一定强 ⑦有单质参加的反应或有单质产生的反应是氧化还原反应 ⑧煤的气化、液化、干馏都是化学变化
A. ④⑤⑧ B. ②③⑤ C. ①④⑥⑦ D. ③④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中不正确的是( )
A.工业上用CO还原赤铁矿(含Fe2O3)获得铁
B.从海产品(如海带等)中提取碘是工业上获取碘的重要途径
C.工业上可通过铝土矿获得铝
D.玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列说法正确的是( )
A.H2 和 H3 属于同素异形体B.C60 的摩尔质量为 720 g
C.O2 和 O4 属于同位素D.N5+离子中含有 36 个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是白色粉末,微溶于水,酸性条件下不稳定,易生成金属 Cu 和Cu2+,广泛应用于化工和印染等行业。某研究性学习小组拟热分解 CuC122H2O 制备 CuCl,并进行相关探究。下列说法正确的是( )

A. 途径 1 中产生的Cl2 可以回收循环利用,也可以通入饱和CaCl2 溶液中除去
B. 途径 2 中 200℃时反应的化学方程式为:Cu2(OH)2Cl2![]() 2CuO+2HCl↑
2CuO+2HCl↑
C. X 气体可以是N2,目的是做保护气,抑制 CuCl22H2O 加热过程可能的水解
D. CuCl 与稀硫酸反应的离子方程式为:2CuCl+4H++SO42—=2Cu2++2Cl—+SO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①![]() ②石墨③C60④
②石墨③C60④![]() ⑤CH3CH2OH⑥
⑤CH3CH2OH⑥![]() ⑦
⑦![]() ⑧CH3OCH3中:互为同位素;______互为同分异构体_______;互为同素异形体_______(填序号).
⑧CH3OCH3中:互为同位素;______互为同分异构体_______;互为同素异形体_______(填序号).
(2)现有①CaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤冰等五种物质,按下列要求回答:
I.熔化时不需要破坏化学键的是_______,熔点最高的是_________。(填序号)
II.只含有离子键的物质是_________,晶体以分子间作用力结合的是_________。(填序号)
(3)写出下列物质的电子式
①H2O______②NaOH______③NH3______;
(4)写出CO2的结构式______;写出硫原子的原子结构示意图______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从单质氟到碘,下列情况中不能反映出它们的氧化性强弱不同的是( )
A.单质与卤化物之间的置换情况
B.与氢气反应的情况
C.与硝酸银反应生成卤化银的颜色情况
D.与水反应的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国重晶石(含BaSO490%以上)资源丰富,其中贵州省重晶石储量占全国总储量的三分之一。我省某工厂以重晶石为原料,生产“电子陶瓷工业支柱”—钛酸钡( BaTiO3)的工艺流程如下:

查阅资料可知:
①常温下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9
②TiCl4在常温下是无色液体,遇水容易发生水解:TiC14+2H2O=TiO2+4HCl
③草酸氧钛钡的化学式为:BaTiO(C2O4)2·4H2O
请回答下列问题:
(1)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为_________________,此反应的平衡常数K=__________(填写计算结果)。若不考虑CO32-的水解,则至少需要使用_______mol/L的Na2CO3溶液浸泡重晶石才能实现该转化过程。
(2)配制TiC14溶液时通常将TiC14固体溶于浓盐酸再加水稀释,其目的是______________。
(3)可循环使用的物质X是____________(填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:____________________。
(4)写出煅烧草酸氧钛钡晶体的化学方程式:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com