
将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图
中产生H2的体积V(L)与时间t(min)的关系,其中正确的是
 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
⑴ Y在元素周期表中的位置为________________。
⑵ 上述元素的最高价氧化物对应的水化物酸性最强的是_______________(写化学式),非金属气态氢化物还原性最强的是__________________(写化学式)。
⑶ Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
⑷ X2M的燃烧热ΔH = -a kJ·mol-1 ,写出X2M燃烧热的热化学方程式:
_____________________________________________________________________。
⑸ ZX的电子式为___________;ZX与水反应放出气体的化学方程式为_______________。
⑹ 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:
 2Z + FeG2
2Z + FeG2 Fe + 2ZG
Fe + 2ZG
放电时,电池的正极反应式为_______________________:
充电时,_____________(写物质名称)电极接电源的负极,该电池的电解质为___________________。
II. 如图是甲烷燃料电池原理示意图,回答下列问题:
(1)电池的负极是__________(填“a”或“b”),该极的电极反应是:__________。

(2)电池工作一段时间后电解质溶液的pH__________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
I:已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:
T℃时物质的浓度(mol•L-1)变化
| 时间/ min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的。第4~5min之间,改变的条件是 ,T℃时该化学反应的平衡常数是 。
在该温度下,若向一容积固定的密闭容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2和2.0mol H2,则反应向 进行。(填“正反应方向”或“逆反应方向”)
(2)已知420℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol•L-1,则CO在此条件下的转化率为 ,如果保持体积不变向该密闭容器中再充入1 mol氩气,平衡时CO的转化率 (填“变大”“不变”“变小”)
(3)397℃时该反应的平衡常数为12,请判断该反应的△H 0(填“>”、“=”、“<”).
II:工业上可用CO和H2在一定条件下合成甲醇,反应为:
CO(g)+2H2(g)⇌ CH3OH(g)ΔH=Q kJ•mol-1
现在容积均为2L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
 |
(1)该反应的Q 0(选填“<”、“>”或“=”,下同),K1 K2。
(2)300℃时,该反应的平衡常数为 。
(3)将容器d中的平衡状态转变到容器c中的平衡状态,可采取的措施有:____________
(至少答2种) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是
A.原子序数: X<Y B.原子半径:X<Y
C.离子半径:X>Y D.原子最外层电子数:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公
众关注的焦点。铊的相关信息如下图所示,其中“6s26p1”表示铊原子
有6个电子层,最外层有3个电子。下列有关卡片信息解读不正确的是
A.铊的元素符号为Tl B.铊原子的中子数为204
C.铊位于第六周期ⅢA族 D.铊的金属性比铝的金属性强

查看答案和解析>>
科目:高中化学 来源: 题型:
设C+CO2 2CO(正反应吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应吸热),正反应的反应速率为v1;N2+3H2 2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1 和v2的变化情况为
2NH3(正反应放热),正反应的反应速率为v2。对于上述反应,当温度升高时,v1 和v2的变化情况为
A.v1减小,v2增大 B.同时减小
C.v1增大,v2减小 D.同时增大
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,且气体体积为标况体积):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大___________,
原因是 。
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体
积的下列溶液,你认为可行的是__________。
A.蒸馏水 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液 E.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
据新闻网报道:科学家首次合成第117号元素,被美国《时代》周刊评选为当年十大科学发现。假如第117号元素符号暂时定为Up,下列关于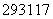 Up和
Up和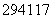 Up的说法中正确的是( )
Up的说法中正确的是( )
A.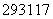 Up和
Up和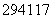 Up是两种元素
Up是两种元素
B.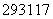 Up和
Up和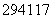 Up互为同位素
Up互为同位素
C.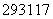 Up和
Up和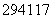 Up质子数不同、中子数相同
Up质子数不同、中子数相同
D.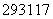 Up和
Up和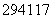 Up质量数相同、电子数不同
Up质量数相同、电子数不同
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。其中Y所处的周期序数与族序数相等。下列说法正确的是( )
| X | |||
| Y | Z | W |
A.原子半径:Y<Z<W
B.气态氢化物的稳定性:X>Z
C.最高价氧化物对应水化物的酸性:Z>W
D.W的最高价氧化物与水反应形成的化合物是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com