
(2)室温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意,回答下列问题。
①若由0.1 mol·L
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol·L-1
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(1)1∶1 (2)①大于或等于 ②大于根据电荷守衡,c(H+)+c(Na+)=c(OH-)+c(A-),由于c(OH-)>c(H+),故c(Na+)>c(A-) ③B C
解析:(1)H2SO4+2NaOH====Na2SO4+2H2O
![]() =10-1 mol·L-1
=10-1 mol·L-1
解得V1=V2
∴V1∶V2=1∶1。
(2)中①所得溶液中溶质仅有NaA,其若为强碱强酸盐,溶液pH=7;若为强碱弱酸盐,水解显碱性,溶液pH>7。②问,由pH>7,可知c(OH-)>c(CH+),再由电荷守恒知c(Na+)+c(H+)=c(OH-)+c(A-),则c(Na+)>c(A-)。③问,常温中性溶液中c(H+)=c(OH-)=1×10-7 mol·L-1,则c(H+)+c(OH-)=2×10-7 mol·L-1,A项说法正确。当HA为弱酸时,若V1=V2,反应后HA过量,所得溶液呈酸性,pH<7,B、C两项说法都不正确。HA可能是强酸,也可能是弱酸,c(HA)≥c(H+)=10-pH mol·L-1=10-3 mol·L-1,而c(NaOH)=c(OH-)=10pH-14 mol·L-1=10-3 mol·L-1,若要混合液呈碱性,NaOH溶液必须过量,则V1一定小于V2,D项说法正确。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 10.0 | 20.0 | 30.0 |
| 生成气体的体积/mL(标准状况) | 89.6 | 179.2 | 224 |
| 16n(H2O2) |
| m(样品) |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将质量比为14︰15的N2和NO混合,混合气体中N2和NO的物质的量之比为 ;氮原子和氧原子的个数之比为 ;该混合气体的平均摩尔质量为 。
(2)23.75g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为 ;则MCl2的相对分子质量为 ;M的相对原子质量为 。
(3)9.2g氮的氧化物(NOx)中含氮原子0.2mol,则(NOx)的摩尔质量为 ;x的数值为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省高三10月月考化学试卷(解析版) 题型:实验题
(共14分)为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
① 甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
② 乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O===2HBr +H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积分数为 。
[探究二]
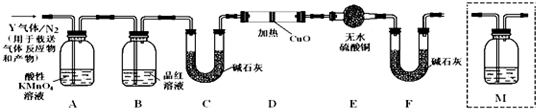
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。

(3)装置B中试剂的作用是
(4)分析Y气体中的Q2气体是如何生成的 (用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于 (选填序号)。
A.A之前 B.A-B间 C.B-C间 D.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com