
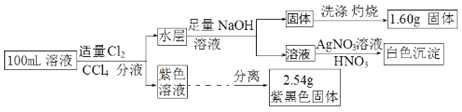
【题目】常温下,有pH=1的某溶液中可能有Na+、Fe3+、Fe2+、I﹣、Cl﹣、CO32﹣中的某几种,现取100mL该溶液进行如下实验:已知氧化性Fe3+>I2,根据实验结果,下列判断正确的是( )
A.Fe3+、I﹣、Cl﹣三种离子一定存在
B.不能确定Na+和Cl﹣是否存在,CO32﹣一定不存在
C.Fe3+与Fe2+至少有一种
D.该溶液中c(Cl﹣)≥0.3molL1
【答案】D
【解析】
pH=1的溶液中存在大量氢离子,则一定不存在CO32-;向溶液中通入氯气、加入CCl4分液后得到紫色溶液,则原溶液中含有I-,Fe3+能够氧化I-,则一定不存在Fe3+;水层中加入氢氧化钠溶液得到固体,该固体洗涤、灼烧得到的1.60g固体为氧化铁,则溶液中一定存在Fe2+,然后结合碘单质的质量、氧化铁的质量及电荷守恒判断氯离子的存在情况及浓度。
pH=1的溶液中氢离子浓度为0.1mol/L,100mL该溶液中含有氢离子的物质的量n(H+)=0.1mol/L×0.1L=0.01mol,由于H+与CO32-会发生离子反应,因此一定不存在CO32-;
向溶液中通入氯气、加入CCl4分液后得到紫色溶液,说明反应产生了I2,原溶液中含有I-,Fe3+能够氧化I-,则一定不存在Fe3+;2.54g紫黑色固体为碘单质,其物质的量n(I2)=2.54g÷254g/mol=0.01mol,则原溶液中含有碘离子的物质的量n(I-)=2n(I2)=0.02mol;
水层中加入NaOH溶液得到固体,该固体洗涤、灼烧得到的1.60g固体为Fe2O3,则溶液中一定存在Fe2+,根据铁元素守恒可知Fe2+的物质的量n(Fe2+)=2n(Fe2O3)=2×![]() =0.02mol,0.02mol Fe2+、0.01molH+共带有正电荷为0.05mol,0.02molI-带有负电荷为0.02mol,根据电荷守恒,原溶液中一定含有Cl-,其物质的量至少为0.04mol-0.02mol+0.01mol=0.03mol,故氯离子的浓度最小c(Cl-)=0.03mol÷0.1L=0.3mol/L。
=0.02mol,0.02mol Fe2+、0.01molH+共带有正电荷为0.05mol,0.02molI-带有负电荷为0.02mol,根据电荷守恒,原溶液中一定含有Cl-,其物质的量至少为0.04mol-0.02mol+0.01mol=0.03mol,故氯离子的浓度最小c(Cl-)=0.03mol÷0.1L=0.3mol/L。
A.根据分析可知,原溶液中一定含有Fe2+、I-、Cl-,A错误;
B.原溶液中一定不存在CO32-,一定含有Cl-,B错误;
C.原溶液中一定存在Fe2+,一定不存在Fe3+,C错误;
D.根据分析可知该溶液中c(Cl-)≥0.3mol/L,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应如下:CO(g)+2H2(g)CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
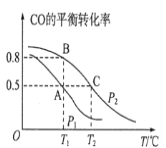
①A、B两点对应的压强大小关系是PA________PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是______。
③下列叙述能说明上述反应能达到化学平衡状态的是__(填代号)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变 c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=___,再加入1.0molCO后重新到达平衡,则CO的转化率__(填“增大,不变或减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灼热的焦炭与水蒸气反应所得产物为H2、CO和少量CO2,为了检验产物中的H2和CO(设气体均被充分吸收),设计如下实验装置。下列有关说法错误的是
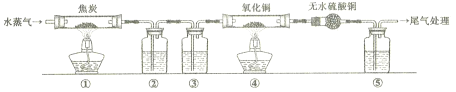
A. 为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
B. ②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
C. ④中黑色固体变红色,即可证明产物中一定含有H2和CO中的一种或两种
D. 若用碱石灰替换无水硫酸铜,也可以达到检验H2和CO目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,反应:A(s)+2B(g)![]() C(g) +D(g)。下列不能表明反应
C(g) +D(g)。下列不能表明反应
达到平衡状态的是( )。
A.气体的压强不变B.气体平均相对分子质量不变
C.气体的密度不变D.B物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子均属于极性分子且中心原子均为sp3杂化的是()
A. NH3、H2O B. SO2、SCl2 C. PCl3、SO3 D. CH4、P4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中通常以加热乙醇和浓硫酸的混合液来制取乙烯,在这个反应里浓硫酸
A.既是反应物又是脱水剂B.既是反应物又是催化剂
C.既是催化剂又是脱水剂D.仅是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积固定的密闭容器中,加入1 molCO2,2 molH2进行吸热反应![]() ,下列情况能说明反应一定达到平衡状态的是
,下列情况能说明反应一定达到平衡状态的是
A. 容器内混合物的相对分子质量不再随时间改变B. 生成1 mol H—H键的同时消耗1 mol CO2
C. 容器内的气体总压强不再随时间改变D. 容器内CO2与H2的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2 L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)![]() C(g)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )
C(g)+xD(g) ΔH>0,容器中A、B、D的物质的量随时间的变化如图所示。下列说法正确的是( )

A.反应前10 min内反应的平均速率为v(D)=0.3 mol·L-1·min-1
B.若平衡时保持温度不变,压缩容器体积,平衡逆向移动,平衡常数K值减小
C.反应至15 min时,其他条件不变,改变的条件可能是缩小容器体积
D.反应至15 min时,其他条件不变,改变的条件可能是降低反应体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行实验,不能达到相应实验目的是()
A.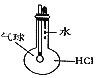 如图装置:验证HCl气体在水中的溶解度大
如图装置:验证HCl气体在水中的溶解度大
B.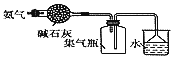 如图装置:可干燥、收集氨气,并吸收多余的氨
如图装置:可干燥、收集氨气,并吸收多余的氨
C.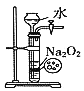 如图装置:制备少量
如图装置:制备少量![]()
D.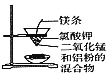 如图装置:可制得金属锰
如图装置:可制得金属锰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com