
【题目】一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表如示。下列判断中正确的是
甲 | 乙 | 丙 | 丁 | ||
容器的体积/L | 2 | 2 | 2 | 1 | |
起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
SO2的平衡转化率% | 80 | α1 | α2 | α3 | |
A. 甲中反应的平衡常数小于乙 B. 该温度下,该反应的平衡常数K为400
C. SO2的平衡转化率:α1>α2=α3 D. 容器中SO3的物质的量浓度:丙=丁<甲
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制2.0 mol/L的NaOH溶液480 mL:

(1)配制时,必须使用的玻璃仪器有烧杯、胶头滴管、_____________、______________。
(2)要完成本实验该同学应称出NaOH ____________ g
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为_____________g
(4)使用容量瓶前必须进行的一步操作是__________________
(5)在配制过程中其他操作都是正确的,下列操作会引起误差偏高的是___________。
A.没有洗涤烧杯和玻璃棒
B.未冷却到室温就将溶液转移到容量瓶并定容
C.容量瓶不干燥,含有少量蒸馏水
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 ( )
A. H2O(g) === H2(g)+ ![]() O2(g) △H=+242kJmol-1
O2(g) △H=+242kJmol-1
B. 2H2(g)+O2(g) === 2H2O(l) △H=-484kJmol-1
C. 2 H2(g)+ O2(g) === 2H2O(g) △H=+242kJmol-1
D. 2H2(g)+O2(g) === 2H2O(g) △H=+484kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法不正确的是

A. b为正极,电极反应式为:O2+2H2O+4e-=4OH-
B. 电解质溶液中的H+移向b电极
C. 若有0.4mol电子转移,则在标准状况下消耗2.24L氧气
D. 呼出气体中酒精含量越高,微处理器中通过的电流越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在发射“神舟”七号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:N2H4(l)+2H2O2(l)===N2(g)+4H2O(g)ΔH=-641.6 kJ·mol-1
H2O(l)===H2O(g) ΔH=+44 kJ·mol-1若用3.2 g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为_______。该反应的热化学方程式为_________________________。
Ⅱ.(1)已知H2(g)+Br2(l)===2HBr(g) ΔH=-72 kJ·mol-1。蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
H2(g) | Br2(g) | HBr(g) | |
1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为_________________。
A.404 B.260 C.230 D.200
(2)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料。
已知:H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 C(s)+![]() O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g) ΔH<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) ΔH<0。一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/ mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正)
C. 保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,到达平衡时,n(Z)=0.24 mol
D. 该温度下此反应的平衡常数:K=14.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是( )
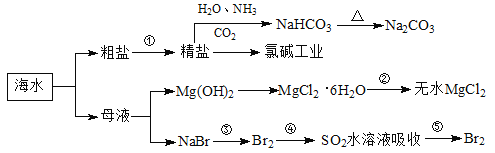
A. 制取NaHCO3的反应是利用其溶解度小于NaCl
B. 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C. 在第③、④、⑤步骤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com