
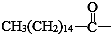 后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的( )
后,苦味消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的( )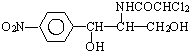
| A. | 无味氯霉素的分子式为:C27H44O6N2Cl2 | |
| B. | 它的水溶性变差,所以苦味消失 | |
| C. | 它是棕榈酸的盐类 | |
| D. | 它的水溶性变良,所以苦味消失 |
科目:高中化学 来源: 题型:解答题
 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mL pH=10的氨水和100mLpH=4的甲酸溶液导电性相同 | |
| B. | pH均为5的HCl和NH4Cl溶液中,水的电离程度相同 | |
| C. | 稀释pH=10的氨水,溶液中所有离子的浓度均降低 | |
| D. | 分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合物中铁单质物质的量的范围:0.03 mol<n(Fe)<0.07 mol | |
| B. | 往得到的溶液中加入NaOH溶液现象为白色沉淀转化为灰绿色最后变为红褐色 | |
| C. | n(Fe)<n(Fe2O3) | |
| D. | 反应后所得溶液中的Fe2+与Cl-的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
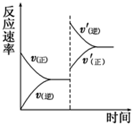 在密闭容器中,一定条件下进行反应:mA(g)+nB(g)?pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,v正、v逆随时间变化过程均如图所示,下列有关叙述正确的是( )
在密闭容器中,一定条件下进行反应:mA(g)+nB(g)?pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,v正、v逆随时间变化过程均如图所示,下列有关叙述正确的是( )| A. | 正反应是吸热反应,m+n>p+q | B. | 逆反应是吸热反应,m+n>p+q | ||
| C. | 正反应是吸热反应,m+n<p+q | D. | 逆反应是吸热反应,m+n<p+q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl与KOH+CH3COOH | B. | NaOH+H2SO4与 Ba(OH)2+H2SO4 | ||
| C. | BaCl2+H2SO4与Ba(OH)2+Na2SO4 | D. | CaCO3+H2SO4 与Na2CO3+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4:3 | B. | 7:3 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:选择题
在日常生活中,我们经常看到铁制品生锈、钒制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是 ( )

A.按图I装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图II是图I所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电 极反应:2Cl--2e-=Cl2↑
极反应:2Cl--2e-=Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com