
【题目】利用硫铁矿(主要成分FeS2)生产硫酸和绿矾(FeSO47H2O)的工业流程示意图如图: 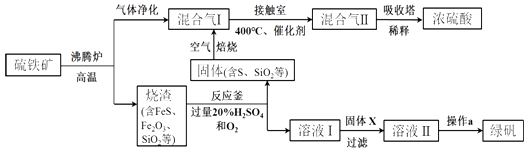
(1)沸腾炉中,硫铁矿进行粉碎处理的目的是 .
(2)接触室中,发生的主要反应是SO2与O2的反应,其化学方程式是 .
(3)反应釜中,烧渣经过反应转化为溶液I和固体. ①烧渣中的FeS在反应中做剂(填“氧化”或“还原”).
②溶液I中所含溶质的化学式是
(4)操作a的主要步骤是:加热浓缩、、过滤洗涤.
(5)流程中,固体X可以选择硫铁矿(FeS2)或;当固体X为硫铁矿(FeS2)时,将溶液I与固体X发生反应的离子方程式补充完整: FeS2++═Fe2++SO42﹣+ .
【答案】
(1)增大反应物的接触面积,提高化学反应速率
(2)2SO2+O2 ![]() 2SO3
2SO3
(3)还原;Fe2(SO4)3、H2SO4
(4)冷却结晶
(5)Fe;14Fe3+;8H2O;16H+
【解析】解:(1)沸腾炉中,硫铁矿进行粉碎处理的目的是使固体与气体充分接触,加快反应速率, 故答案为:增大反应物的接触面积,提高化学反应速率;(2)接触室中,SO2与O2的反应生成SO3 , 反应的化学方程式为2SO2+O2 ![]() 2SO3 ,
2SO3 ,
故答案为:2SO2+O2 ![]() 2SO3;(3)①反应釜中的FeS被氧化成硫,所以FeS在反应中做还原剂,
2SO3;(3)①反应釜中的FeS被氧化成硫,所以FeS在反应中做还原剂,
故答案为:还原;②根据上面的分析可知,溶液Ⅰ主要成分为硫酸铁及过量的硫酸,其化学式为Fe2(SO4)3、H2SO4 ,
故答案为:Fe2(SO4)3、H2SO4;(4)操作a为从硫酸亚铁溶液中获得硫酸亚铁晶体,其操作为加热浓缩、冷却结晶、过滤洗涤,
故答案为:冷却结晶;(5)流程中,固体X主要目的是将铁离子还原成亚铁离子,所以X可以是FeS2或Fe,硫铁矿(FeS2)与硫酸铁发生氧化还原反应生成亚铁离子和硫酸根离子,反应的离子方程式为FeS2+14Fe3++8H2O═15Fe2++2SO42﹣+16H+ ,
故答案为:Fe;14Fe3+、8H2O、16H+ .
硫铁矿在沸腾炉中高温生成氧化铁与二氧化硫,混合气体Ⅰ为二氧化硫和空气,经过接触室后二氧化硫被氧化成三氧化硫,所以混合气体Ⅱ为三氧化硫、二氧化硫、空气等,沸腾炉中产生的炉渣主要为硫化亚铁、氧化铁、二氧化硅等,加入硫酸溶解,再用氧气氧化可得溶液Ⅰ主要成分为硫酸铁,硫酸铁中加入铁粉得溶液Ⅱ为硫酸亚铁溶液,经蒸发浓缩、冷却结晶得到硫酸亚铁晶体,烧渣用酸溶解后得固体主要成分为二氧化硅和硫,硫经氧化得二氧化硫,可循环利用,(1)固体粉碎处理可使固体与气体充分接触,加快反应速率;(2)接触室中,SO2与O2的反应生成SO3;(3)①反应釜中的FeS被氧化成硫,据此答题;②根据上面的分析可知,溶液Ⅰ主要成分为硫酸铁及过量的硫酸;(4)操作a为从硫酸亚铁溶液中获得硫酸亚铁晶体,可以用降温结晶的方法;(5)流程中,固体X主要目的是将铁离子还原成亚铁离子,据此书写离子方程式.


科目:高中化学 来源: 题型:
【题目】室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( ) 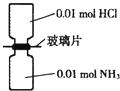
A.反应前气体的总体积为0.448L
B.装置中氢元素的总质量为0.04g
C.生成物中含有0.01NA个分子
D.生成物完全溶于水后所得溶液含有0.01 NA个NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是( )
加入的物质 | 结论 | |
A | 50mL 1mol/L H2SO4 | 反应结束后,c(Na+)=c(SO42﹣) |
B | 0.5mol CaO | 溶液中 |
C | 50mL H2O | 由水电离出的c(H+)c(OH﹣)不变 |
D | 0.1mol NaHSO4固体 | 反应完全后,溶液pH减小,c (Na+)不变 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.沸点由低到高的顺序为:CH3CH2CH3<CH3(CH2)2CH3<(CH3)3CH
B.工业上合成 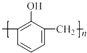 的单体为甲醛和苯酚(
的单体为甲醛和苯酚( ![]() )
)
C.相同质量的乙烯和乙酸完全燃烧时,消耗氧气的量相同
D.某烷烃可以命名为2,3,3﹣三甲基﹣4﹣乙基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L的H2A溶液体系中,含A粒子的分布系数(平衡时某粒子的浓度占各粒子浓度之和的分数)与溶液 pH的关系如图所示.下列说法不正确的是( ) 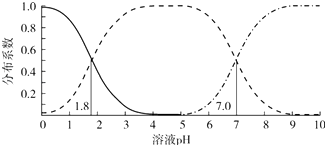
A.室温下,HA﹣的电离常数Ka2=1.0×10﹣7
B.室温下,0.1mol/L的NaHA溶液显酸性
C.室温下,0.2mol/L的H2A与0.1mol/L的NaOH溶液等体积混合,溶液pH=1.8
D.0.1mol/L的Na2A溶液中c(OH﹣)=c(H+)+c(HA﹣)+2c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是( )
A.使酚酞试液变红的溶液:Na+、Cl﹣、SO ![]() 、Fe3+
、Fe3+
B.常温下 ![]() =0.1mol?L﹣1的溶液:K+、Na+、SiO
=0.1mol?L﹣1的溶液:K+、Na+、SiO ![]() 、NO
、NO ![]()
C.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、MnO ![]() 、Cl﹣
、Cl﹣
D.澄清透明溶液:Al3+、Na+、SO ![]() 、HCO3﹣
、HCO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com