
【题目】室温下,用0.100molL-1NaOH溶液分别滴定20.00mL0.100molL-1的HA和HB两种酸溶液,滴定曲线如图所示[已知AG=lg![]() ],下列说法不正确的是( )
],下列说法不正确的是( )

A.P点时,加入NaOH溶液的体积为20.00mL
B.Ka(HB)的数量级为10-4
C.水的电离程度:N>M=P
D.M、P两点对应溶液中存在:c(A-)=c(B-)
【答案】D
【解析】
未加NaOH溶液时,HA的AG=12,则c(H+)c(OH-)=10-14,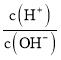 =10-12,则c(H+)=0.1mol/L=c(HA),HA是强酸;
=10-12,则c(H+)=0.1mol/L=c(HA),HA是强酸;
未加NaOH溶液时,HB的AG=9,则c(H+)c(OH-)=10-14,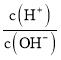 =10-9,则c(H+)=10-2.5mol/L<0.1mol/L,则HB是弱酸;
=10-9,则c(H+)=10-2.5mol/L<0.1mol/L,则HB是弱酸;
A.P点AG=0时,c(H+)=c(OH-),混合溶液呈中性,HA是强酸,酸碱的物质的量相等,酸碱的物质的量浓度相等,则酸碱体积相等,所以加入NaOH溶液的体积为20.00mL,故A正确;
B.HB的电离程度较小,则溶液中c(B-)≈c(H+)=10-2.5mol/L,c(HB)≈0.1mol/L,Ka(HB)=![]() =
=![]() =10-4,故B正确;
=10-4,故B正确;
C.酸或碱抑制水电离,弱离子促进水电离,且酸中c(H+)越大其抑制水电离程度越大,M、P点溶液都呈中性,则M、P点不影响水的电离,N点NaB浓度较大,促进水电离,所以水的电离程度:N>M=P,故C正确;
D.M、P点的AG都为0,都存在c(H+)=c(OH-),混合溶液呈中性,加入的NaOH越多,c(Na+)越大,溶液中存在电荷守恒,则存在P点c(A-)=c(Na+)、M点c(Na+)=c(B-),但是c(Na+):M<P点,则c(A-)>c(B-),故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】以铬铁矿(含FeO·Cr2O3、Al2O3、SiO2等)为原料制备二草酸铬钾的实验步骤如图:
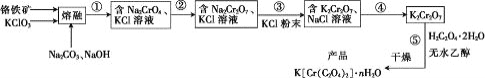
回答下列问题:
(1)“熔融”的装置如图,坩埚W的材质可以是________(填“铁”“陶瓷”或“玻璃”);FeO·Cr2O3与KClO3及Na2CO3发生反应,生成Fe2O3、KCl、Na2CrO4和CO2的化学方程式为_______________。
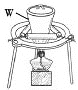
(2)熔融后的固体中含Na2CrO4、Fe2O3、Na2SiO3、NaAlO2、KCl等,步骤①的具体步骤为水浸,过滤,调pH为7~8,加热煮沸半小时,趁热过滤。第一次过滤滤渣中的主要成分为________,“调pH为7~8,加热煮沸半小时”的目的是__________。
(3)步骤②需加入酸,则加入稀硫酸时发生反应的离子方程式为________。
(4)步骤④包含的具体操作有____,经干燥得到K2Cr2O7晶体。(有关物质的溶解度曲线如图所示)
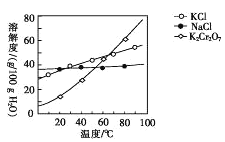
(5)步骤⑤需往两种固体混合物中加入一滴水及少量酒精研磨,所用的硅酸盐质仪器的名称是________。
(6)采用热重分析法测定K[Cr(C2O4)2]·nH2O样品所含结晶水数目,将样品加热到80℃时,失掉全部结晶水,失重16.8%。K[Cr(C2O4)2]·nH2O晶体中n=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年是元素周期表诞生 150 周年,目前周期表七个周期均已排满,其 118 种元素。短周期元素 W、X、Y、Z在周期表中的相对位置如图所示,且 W 元素的简单氢化物的空间结构是三角锥形,下列说法不正确的是
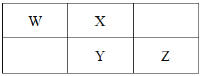
A.红葡萄酒含有 YX2,起杀菌、澄清、抗氧化的作用
B.在元素周期表中,117 号元素与 Z 元素位于同一主族
C.简单离子的半径大小顺序为:X < W < Z < Y
D.W 的氢化物与 Z 的氢化物反应,产物为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的是
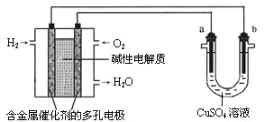
A. 燃料电池工作时,负极反应为:H2—2e-= 2H+
B. 若要实现铁上镀铜,则a极是铁,b极是铜
C. 若要实现电解精炼粗铜,则a极发生氧化反应, b极质量增加
D. 当a、b均是石墨时,当消耗H2 22.4L(标况)时,a极析出铜64g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用固体KOH配制0.1 mol/L的KOH溶液 480 mL,回答下列问题:
(1)配制过程中需要用到的玻璃仪器有______。
(2)需要用托盘天平称量______g KOH固体。
(3)如果在定容时仰视操作,则所配得溶液的浓度______0.1 mol/L(填>,=,<)。
(4)若所用的固体KOH中混有NaOH,则所配得溶液的c(OH-)浓度______0.1 mol/L (填>,=,<)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值.下列说法正确的是
A.0.1 mol 的11B中,含有0.6NA个中子
B.pH=1的H3PO4溶液中,含有0.1NA个H+
C.2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子
D.密闭容器中2 mol SO2与1 molO2反应制得2 molSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3 个能级上有电子,且每个能级上的电子数相等,B原于核外电子有7 种不同的运动状态,C元素原于核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价层电子均已成对。
回答下列问题:
(1)E2+ 的价层电子排布图为_____________________。
(2)五种元素中第一电离能最小的是_______________(填元素符号),CAB-离子中,A原子的杂化方式是______________________。
(3)AB-、D+ 和E2+三种离子组成的化学物质D2E(AB)4,其中化学键的类型有_______,该化合物中存在一个复杂离子,该离子的化学式为_________________,配位体是_____________________。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。

①该化合物的化学式为________,E的配位数为______________,C采取_______(填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积。
②列式表示该晶体的密度:_______________ g·㎝-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向NaX溶液和YCl溶液中加入盐酸和氢氧化钠溶液,混合溶液的PH与离子浓度变化关系如图所示,下列说法不正确的是( )
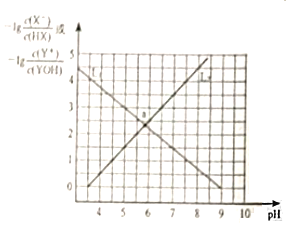
A.0.1mol/L的YX溶液中离子浓度关系为:c(Y+)>c(X-)>c(OH-)>c(H+)
B.L1表示-lg![]() 与pH的变化关系
与pH的变化关系
C.Kb(YOH)=10-10.5
D.a点时两溶液中水的电离程度不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com