
| A、溶液的pH增加 |
| B、促进CH3COOH的电离 |
| C、溶液的导电能力减弱 |
| D、溶液中c(OH-)减少 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、欲证明放入硫酸溶液中的纤维素加热已发生水解,可向所得溶液加入银氨溶液,放在水浴中 |
| B、欲证明淀粉的水解产物为葡萄糖,可向试管中加入0.5克淀粉及20%的稀硫酸4ml,加热3-4分钟,再向试管中加入新制Cu(OH)2 煮沸,观察有机红色沉淀生成 |
| C、为证明硬脂酸有酸性,取稀NaOH溶液加入硬脂酸并加热 |
| D、用灼烧的方法检验是毛线还是棉线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
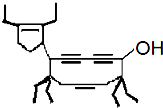 2009年是中国农历牛年,有一种有机物的键线式也酷似牛,故称为牛式二烯炔醇(cowenynenynol).已知连有四个不同的原子或原子团的碳原子,称为手性碳原子.下列有关说法不正确的是( )
2009年是中国农历牛年,有一种有机物的键线式也酷似牛,故称为牛式二烯炔醇(cowenynenynol).已知连有四个不同的原子或原子团的碳原子,称为手性碳原子.下列有关说法不正确的是( )| A、牛式二烯炔醇含有3种官能团 |
| B、牛式二烯炔醇分子内能发生消去反应 |
| C、1mol牛式二烯炔醇最多可与6molBr2发生加成反应 |
| D、牛式二烯炔醇含有3个手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应的氧化剂是偏二甲肼 |
| B、该反应进行时只有放热过程没有吸热过程 |
| C、该反应中氮元素的化合价升高 |
| D、该反应中每生成1mol CO2转移8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
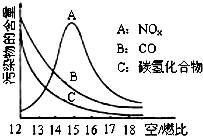 稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.
稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) |
| B、在常温下,10mL 0.02mol/L HCl溶液与10mL 0.02 mol/L Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12 |
| C、在0.1mol/L NH4Cl溶液中:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| D、将0.2mol/L的盐酸与0.1mol/L的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(Na+)<c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2+Mg2+=Mg(OH)2+Ca2+ |
| B、2OH-+Mg2+=Mg(OH)2↓ |
| C、Na2CO3+Ca2+=CaCO3↓+2Na+ |
| D、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入适量的NaBr溶液 |
| B、通入溴蒸气 |
| C、加入适量的NaOH溶液 |
| D、加适量的KI溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com