
【题目】某化学研究性学习小组为学习了元素性质后,分别设计了如下实验:
(1)甲同学想探究“铝热反应”中熔融物的成份,他查阅《化学手册》得到Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | …… |
①由此甲同学推测,教材中铝热反应所得到的熔融物应是铁铝合金。其理由是:_______________。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝,该实验所用试剂是___,反应的离子方程式为_____。
③甲同学为确定熔融物中是否还会有残留的Fe2O3,将熔融物用酸完全溶解后加入KSCN试剂。请你分析该设计是否正确___(填“正确”或“不正确”),理由是(用离子方程式表示)______________________。
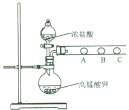
(2) 乙同学设计了如下图装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。乙同学可能观察到的现象有_______。 从环保角度考虑,该装置有明显不足,请提出改进建议_____________________。
(3) 丙同学欲比较N、C、Si的非金属性强弱,设计了下图所示的实验装置,其设计能否达到实验目的______(填“能”或“不能”),理由是______________。 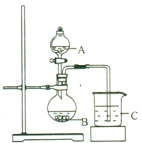
【答案】铝热反应得到熔融态的铁,此温度下铝也为熔融态,二者融合在一起形成铁铝合金 氢氧化钠溶液 2Al+2OH-+2H2O=2A1O2-+3H2 ![]() 不正确 2Fe3++Fe=3Fe2+或3Fe3++Al=A13++3Fe2+ 圆底烧瓶内充满黄绿色气体,A处由无色变橙黄色,B处变蓝,C处褪色 没有尾气处理装置,在C的右端塞入一团沾有浓NaOH溶液的棉花 不能 挥发出的硝酸可能使烧杯内出现浑浊
不正确 2Fe3++Fe=3Fe2+或3Fe3++Al=A13++3Fe2+ 圆底烧瓶内充满黄绿色气体,A处由无色变橙黄色,B处变蓝,C处褪色 没有尾气处理装置,在C的右端塞入一团沾有浓NaOH溶液的棉花 不能 挥发出的硝酸可能使烧杯内出现浑浊
【解析】
(1)①铝的熔点低于铁的熔点、但沸点高于Fe的熔点;
②根据铝与氢氧化钠溶液反应放出氢气设计实验;
③铁、Al能把Fe3+还原为Fe2+;
(2)烧瓶中浓盐酸与高锰酸钾能反应生成氯气;A处NaBr和氯气反应生成氯化钠和溴单质、B 处KI和氯气反应生成氯化钾和碘单质、C处湿润的氯气具有漂白性;氯气有毒,不能直接排放到空气中;
(3)由图所示的实验装置可知,根据强酸制取弱酸的反应比较非金属性,最高价氧化物的水化物酸性越强,对应非金属元素的非金属性越强;
(1)①铝热反应得到熔融态的铁,此温度下铝也可为熔融态,二者融合在一起形成铁铝合金,铝热反应所得到的熔融物应是铁铝合金;
②铝与氢氧化钠溶液反应放出氢气,把铝热反应所得的固体样品放入热氢氧化钠溶液中,若有气泡生成说明样品中含有金属铝,反应离子方程式是2Al+2OH-+2H2O=2A1O2-+3H2 ![]() ;
;
③熔融物中含有铁、Al,铁、Al能把Fe3+还原为Fe2+,将熔融物用酸完全溶解后加入KSCN,若溶液不变红,不能证明熔融物中一定不含Fe2O3,反应的离子方程式是2Fe3++Fe=3Fe2+或Al+3Fe3+=Al3++3Fe2+;
(2) 圆底烧瓶内浓盐酸与高锰酸钾能反应生成氯气,烧瓶中充满黄绿色气体, NaBr和氯气反应生成氯化钠和溴单质,A处蘸有NaBr溶液的棉花由无色变橙黄色;KI和氯气反应生成氯化钾和碘单质,碘遇淀粉变蓝色,所以B处湿润的淀粉KI试纸变蓝;湿润的氯气具有漂白性,所以C处湿润的红纸褪色;氯气有毒,不能直接排放到空气中,不足之处是没有尾气处理装置,改进方法是在C的右端塞入一团沾有浓NaOH溶液的棉花。
(3)较强的酸可以制备较弱的酸,而元素的非金属性越强,最高价氧化物的水化物的酸性就越强,所以可利用硝酸和碳酸钙反应生成CO2,将CO2通入到硅酸盐溶液中生成硅酸沉淀即可以完成实验,该装置存在缺陷是因为硝酸具有挥发性,挥发出的硝酸可能使烧杯内出现浑浊,干扰碳酸与硅酸酸性的比较。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】二甲醚是一种重要的清洁燃料。合成二甲醚是解决能源危机的研究方向之一。
(1)用CO2和H2可以合成二甲醚(CH3OCH3)。
已知:CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.1 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-41.1 kJ·mol-1
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5 kJ·mol-1
则反应2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)ΔH=________。
(2)二甲醚(CH3OCH3)燃料电池可以提升能量利用率。利用二甲醚酸性介质燃料电池电解200 mL饱和食盐水(惰性电极),一段时间后,阴极收集到标况下的氢气2.24 L(设电解后溶液体积不变)。
①二甲醚燃料电池的正极反应式为:___________,负极反应式为:_____________。
②请写出电解食盐水的化学方程式:____________________。
③电解后溶液的c(OH-)=________,理论上消耗二甲醚的质量为________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-VOCl2电池是一种基于阴离子传导的新型二次电池,其简化装置示意图如下。总反应为Mg+2VOCl2![]() MgCl2+2VOCl,下列说法错误的是
MgCl2+2VOCl,下列说法错误的是

A.采用Mg作电极材料比Li的安全性更高
B.为该电池充电时Mg电极应与电源的正极相连
C.放电时正极反应为VOCl2+e-= VOCl+Cl-
D.放电过程中Cl-穿过复合离子液体向Mg移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种常见的燃料,也是重要的基础化工原料。回答下列问题:
(1)采用甲醇气相氨化法可制得二甲胺。
已知:2CH3OH(g)+3O2(g) 2CO2(g)+4H2O(g) H1=-3122kJ/mol
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) H2=-472 kJ/mol
4(CH3)2NH(g)+15O2(g) 8CO2(g)+14H2O(g)+2N2(g) H3=-7492 kJ/mol
则制备二甲胺反应2CH3OH(g)+NH3(g) (CH3)2NH(g)+2H2O(g)的H=_____ kJ/mol。
(2)一定条件下,甲醇气相氨化法原料气中c(CH3OH):c(NH3)分别为1:1、2:1、3:1时,NH3的平衡转化率随温度变化的关系如图:
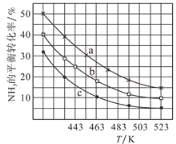
①代表原料气中c(CH3OH):c(NH3)=1:1的曲线是________。
②一定温度下,控制原料气中c(CH3OH):c(NH3)=3:1,能增大NH3平衡转化率的措施是_______。
③温度为443K时,按c(CH3OH):c(NH3)=2:1投料,若NH3的起始浓度为2mol/L,则反应达到平衡时,(CH3)2NH的体积分数为_______,该温度下的化学平衡常数为________ 。
(3)甲醇可通过电化学方法由甲烷直接制得,装置如下图所示,电解生成CH3OH的过程分为3步:

①通电时,氯离子先转化为高活性的原子氯(Cl·);
②Cl·与吸附在电极上的CH4反应生成HCl和CH3Cl;
③在碱性电解液中,CH3Cl转化为目标产物CH3OH。
步骤①的电极反应式为__________,步骤③的离子方程式为__________,维持电流强度为1.5A,装置工作2小时,理论上可制得CH3OH的质量为________g。(已知F=96500C/mol,不考虑气体溶解等因素)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置进行下列实验,试管内试剂可按需要更换,实验不产生污染性气体且能成功的是 ( )

A.加热NaHCO3制CO2,并用澄清石灰水检验CO2
B.用Cu与浓硫酸反应制少量SO2,并检验SO2的漂白性
C.加热NH4Cl制NH3,并检验氨气溶于水后显碱性
D.用醋酸与乙醇、浓硫酸混合反应制乙酸乙酯,并观察生成的乙酸乙酯的状态、气味
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示转化关系中涉及到的物质均由主族元素组成(部分产物已略去),其中C、D为单质,A、B、E、F、G为化合物,除C与D的反应外,其它反应均在溶液中进行。请填写下列空白。
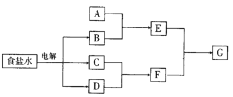
(1) 若A是常见的金属或金属氧化物,当F过量时,G为可溶性盐,则A的化学式为_________或_________。
(2) 若A是一种常见氧化物,不管F过量与否,G为同一种难溶性物质,则A的名称是________,晶体类型是_______,A的用途是_________。
(3) 若A是一种具有漂白性的气态氧化物,A是___;若A是一种无味的气态氧化物,A的电子式为______。
(4) 若A为有机化合物,如果A与G为同一物质,请写出两种A(不同类别物质)的结构简式:_____;_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,2.24 L CHCl3 所含共价键数为0.4NA
B.常温常压下,2 g羟基(18OD)所含的中子数为NA
C.常温常压下,1.5 g NO与1.6 g O2充分反应后混合物中原子总数为0.2NA
D.常温下,2 L 0.1 molL-1FeCl3 溶液与1 L 0.2 molL-1FeCl3 溶液所含Fe3+数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的键线式结构为![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
A.有机物A的分子式为C8H18
B.用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C.有机物A的一氯代物只有4种
D.B的结构可能有3种,其中一种的名称为3,4,4-三甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于碳碳双键不能自由旋转,因此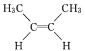 和
和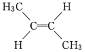 是两种不同的化合物,二者互为顺反异构体。则分子式为C3H4Cl2且含有碳碳双键的同分异构体(含顺反异构)有( )
是两种不同的化合物,二者互为顺反异构体。则分子式为C3H4Cl2且含有碳碳双键的同分异构体(含顺反异构)有( )
A. 7种B. 5种C. 6种D. 4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com