
市售氯化钾中所含杂质以Na+、Mg2+为主,也含有少量SO42—、Fe3+等。提纯过程如下:
(1)操作I所用的玻璃仪器有 ;操作II的主要步骤是 。
(2)滤渣a的主要成分是 ;滤渣b的主要成分是 。
(3)检验BaCl2溶液是否加入过量,其详细操作过程为 。
(4)产品KCl晶体可能仍含少量的NaCl,进一步提纯的方法是 。
(16分)
(1)漏斗、烧杯、玻璃棒(3分) 蒸发浓缩、冷却结晶、过滤洗涤烘干(3分)
(2)Mg(OH)2、Fe(OH)3、BaSO4(3分) CaCO3、BaCO3(2分)
(3)向上层清液中滴加几滴BaCl2溶液,若有沉淀生成,则未过量,若无沉淀生成,则已过量(3分)
(4)重结晶(2分)
解析试题分析:(1)根据操作I的目的是从混合物中分离滤渣和溶液,说明I是过滤,需要使用烧杯、漏斗、玻璃棒;II的目的是从B溶液中制取KCl晶体,说明II是结晶,主要步骤为蒸发浓缩、冷却结晶、过滤、洗涤、烘干;(2)加入过量石灰水,其中的氢氧根与铁离子、镁离子分别结合成氢氧化铁沉淀、氢氧化镁沉淀,加入过量氯化钡溶液,其中的钡离子与硫酸根离子结合生成硫酸钡沉淀,但它们引入钙离子、氢氧根、钡离子等新杂质,则滤渣a的主要成分Fe(OH)3、Mg(OH)2、BaSO4;溶液a中加入过量的K2CO3时,其中的碳酸根离子与钙离子、钡离子分别结合生成碳酸钙沉淀、碳酸钡沉淀,但是引入的碳酸根离子是新杂质,则滤渣b的主要成分是CaCO3、BaCO3;(3)将悬浊液A静置之后,向上层清液中滴加几滴BaCl2溶液,若有白色沉淀生成,则BaCl2未过量,若无白色沉淀生成,则BaCl2已过量;(4)对于已经使用结晶法制取的氯化钾晶体,除去其中所含少量NaCl的方法是重结晶。
考点:考查物质制备化学工艺流程,涉及混合物分离提纯方法及步骤、使用的仪器、滤渣成分、设计实验方案判断除杂试剂是否过量等。


科目:高中化学 来源: 题型:实验题
S2Cl2是工业上常用的硫化剂,实验室制备的方法有2种: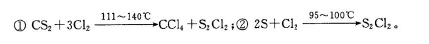 已知在S2Cl2中硫元素显+1价,电子式:
已知在S2Cl2中硫元素显+1价,电子式: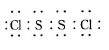 ,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下: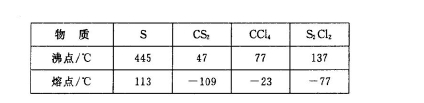
实验室利用下列装置制备 (部分夹持仪器已略去):
回答下列问题:
(1)写出A装置中发生反应的离子方程式
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是
(3)D中冷凝管起到导气和冷凝回流双重作用。这种冷却装置可应用于下列高中化学中 实验。
| A.石油分馏 | B.制备乙烯 | C.制取乙酸乙酯 | D.制取溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
无水氯化铝是一种重要的有机合成催化剂,还可用于金属冶炼、润滑油合成;食品级无水氯化铝也可用作膨松剂、絮凝剂等。
某研究性学习小组查阅资料后利用下图所示装置制备无水氯化铝。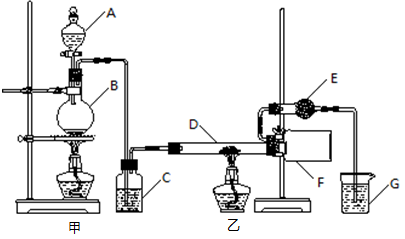
资料显示:氯化铝为无色透明晶体或白色而微带浅黄色的结晶性粉末,在178℃升华,其蒸气是缔合分子(Al2Cl6),在空气中能吸收水分,发生水解。
(1)填写下列仪器的名称:A ,B 。
(2)装置C中盛装的试剂是 ;装置G中盛装的试剂是 。
(3)相同条件下,氯化铝蒸气对氢气的相对密度是 。
(4)装置F中的现象是 。
(5)装置E的作用是 。
(6)实验结束后应先撤去 (填“甲”或“乙”)处的酒精灯。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
利用如图装置探究氯气和氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为较纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式为 。
(2)装置A中的烧瓶内固体宜选用 (选填以下选项的代号)
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)按A接B接C;F接E接D接C,请在各虚线框内画上合适的装置图并注明所装试剂名称:
(4)在C中观察到大量白烟,同时产生一种气体单质,该反应的化学方程式为 ,反应中氧化剂与还原剂的物质的量比为 。设计一个实验方案鉴定该固体是氯化铵(要求写出操作、现象及结论): 。
(5)从装置C的G处逸出的尾气可能含有污染环境的气体,如何处理:
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氮及其化合物在生产、生活中有重要的作用。
(1)NH3是制碱工业中不可缺少的重要物质。继侯德榜“联合制碱法”后,上世纪50年代某些化工专家开始研究有机胺制碱法,其工艺流程如下: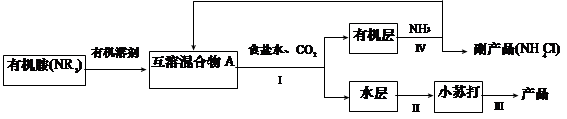
已知:NR3 + CO2 + NaCl + H2O = NaHCO3 + NR3·HCl
NR3 + HCl = NR3·HCl,且NR3·HCl 易溶于有机溶剂。
①操作Ⅰ名称为 ;
②某实验小组同学查阅资料知,有机溶剂和有机胺沸点差别较大,现欲将A中各成分进行分离,请写出除了导管、酒精灯、牛角管、锥形瓶外,该分离操作所需的玻璃仪器名称 ;
(2)N2在化工生产、农业、医疗、航天航空等领域用途广泛。现提供以下装置(连接仪器略去):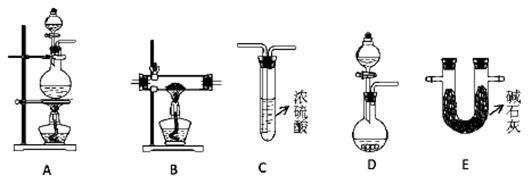
①某化学兴趣小组甲同学欲用加热NaNO2 和NH4Cl的浓溶液制得N2,应该选择的发生装置是 ,检验该发生装置气密性的操作为 ;
②在加热条件下,用NH3 还原CuO可制得N2,同时获得铜粉,此反应的化学方应方程式是 。乙同学用此法制得干燥、纯净的N2,且需要的NH3 以生石灰和浓氨水作原料。按气流从左到右,整套装置的连接顺序是 (填写字母序号);最后一个装置中试剂的作用是 ;
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室制乙烯时,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯, 加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| …… | |
| 实验完毕, 清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
| | 设 计 | 现 象 |
| 甲 | 在A、B间增加一个装有某种试剂的洗气瓶 | Br2的CCl4溶液褪色 |
| 乙 | 与A连接的装置如下: | D中溶液由红棕色变为浅红棕色时,E中溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
无水FeCl3呈棕红色,极易潮解,100℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
请回答:
(1)装置A中反应的离子方程式为 。
(2)装置F中所加的试剂为 。
(3)导管b的作用为 ;
装置B的作用为 。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为 。
(5)反应结束后,拆卸装置前,必须进行的操作是
(6)为检验所得产品中是否含有FeCl2,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入一种试剂,该试剂为 (填序号)。
①Fe粉 ②KSCN溶液 ③酸性KMnO4溶液 ④NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验操作正确且能达到预期目的的是
| | 实验目的 | 操作 |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入酸性KMnO4溶液,看紫红色是否褪去 |
| C | 确定碳、氯两元素非金属性的强弱 | 测定同温同浓度的Na2CO3和NaClO水溶液的pH |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是 ( )。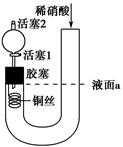
| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com