
【题目】如图是常温下部分短周期元素,最高价氧化物对应水化物的等物质的量浓度稀溶液的pH值与原子序数的关系图,其中H的氧化物是两性氧化物。下列说法正确的是

A. 元素B对应的氢化物比J对应的氢化物熔沸点更高,原因是B的氢化物中的键能比J中的大。
B. 根据图形分析可知,K、L两种元素最高价氧化物对应的水化物的酸性,前者较强。
C. 晶体IC2熔化时克服的化学键和晶体KC2与水反应时克服的化学键,类型相同。
D. 元素K、H、G分别形成的简单离子的半径逐渐减少
【答案】C
【解析】图中所列元素均为短周期元素,F. G、H的最高价氧化物对应水化物呈碱性,A. B. I、J、K、L的最高价氧化物对应水化物呈酸性,其中H的氧化物是两性氧化物,则H为Al,由溶液pH及原子序数,可推知A为碳、B为氮、C为氧、D为氟、E为Ne、F为Na、G为Mg、I为Si、J为P、K为S、L为Cl。
A. 由于NH3分子之间存在氢键,沸点高于PH3,与键能无关,故A错误;B. 常温下相同浓度时,硫酸溶液的pH较小(比较氢离子浓度),但从电离的难易程度和元素非金属性的强弱比较,高氯酸的酸性强于硫酸,故B错误;C. 晶体SiO2属于原子晶体,熔化时克服共价键,晶体SCl2属于共价化合物,与水反应时克服共价键,故C正确;D. 电子层结构相同的离子,核电荷数越大离子半径越小,电子层结构不同的离子,电子层数越多离子半径越大,故离子半径:S2>Mg2+>Al3+,故D错误;答案选C。


科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述不正确的是( )

A. 汉黄芩素的分子式为C16H12O5
B. 该物质遇FeCl3溶液显色
C. 1mol该物质与溴水反应,最多消耗2mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2SO3·CuSO3·2H2O是一种深红色固体(以下用M表示)。某学习小组拟测定胆矾样品的纯度,并以其为原料制备M。
已知:①M不溶于水和乙醇,100℃时发生分解反应;
②M可由胆矾和SO2为原料制备,反应原理为3Cu2++6H2O+3SO2![]() Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
Cu2SO3·CuSO3·2H2O↓+8H++SO42-。
I.测定胆矾样品的纯度。
(1)取w g胆矾样品溶于蒸馏水配制成250mL溶液,从中取25.00mL于锥形瓶中,加入指示剂,用c mol·L-1EDTA(简写成Na4Y)标准溶液滴定至终点(滴定原理:Cu2++Y4-====CuY2-),测得消耗了V mL EDTA标准溶液。则该胆矾样品的纯度为____________%(用含c、V、w的代数式表示)。如果滴定管装液前没有用EDTA标准溶液润洗,测得的结果会_________ (填“偏高”“偏低”或“无影响”)。
Ⅱ.制备M。实验装置如下图所示:

(2)实验室用70%硫酸与亚硫酸钠粉末在常温下制备SO2。上图A处的气体发生装置可从下图装置中选择,最合适的是________(填字母)。

(3)装置D中的试剂是____________。装置B中水浴加热的优点是____________________。
(4)实验完毕冷却至室温后,从锥形瓶中分离产品的操作包括:__________、水洗、乙醇洗、常温干燥,得产品Cu2SO3·CuSO3·2H2O。检验产品已水洗完全的操作是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4 , 无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
(1)联氨分子的电子式为 , 其中氮的化合价为 .
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 .
(3)①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=﹣1048.9kJmol﹣1
上述反应热效应之间的关系式为△H4= , 联氨和N2O4可作为火箭推进剂的主要原因为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)天然气和可燃冰(mCH4nH2O)既是高效洁净的能源,也是重要的化工原料。
①可燃冰(mCH4nH2O)属于_____晶体,写出CH4的结构式______。
②已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.65kJ热量,则该条件下反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的 △H=___kJ/mol。
(2)用甲烷--氧气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。反应装置如下图所示:

①b电极名称为______,d电极的电极反应式为__________。
②假设CuCl2溶液足量,当某电极上析出3.2g金属Cu时,理论上燃料电池消耗的氧气在标准状兄下的体积是_______mL。
(3)25℃,101kPa条件下,14gN2和3gH2反应生成NH3的能量变化如下图所示:
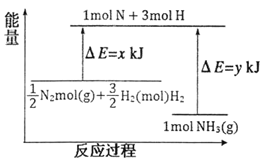
已知:①x=1127;
②25℃,101kPa下,N2(g)+3H2(g)![]() 2NH3(g) △H=-92kJmol-1。则y=______。
2NH3(g) △H=-92kJmol-1。则y=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂.以下是一种制备过氧化钙的实验方法.回答下列问题:
(1)碳酸钙的制备(如图1) 
(i)步骤①加入氨水的目的是调节溶液pH使Fe(OH)3沉淀,小火煮沸的作用是使沉淀颗粒长大,有利于 .
(ii)如图是某学生的过滤操作示意图,其操作不规范的是(填标号).
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加过过滤速度
(2)过氧化钙的制备(如图3) 
(i)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈性(填“酸”、“碱”或“中”).将溶液煮沸,趁热过滤,将溶液煮沸的作用是 .
(ii)步骤③中反应的化学方程CaCl2+2NH3·H2O+H2O2+6H2O=CaO28H2O↓+2NH4Cl该反应需要在冰浴下进行,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素C和Si的非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,图2中A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)从以下所给物质中选出甲同学设计的实验所用到物质:图1中试剂A、B为(填序号)____;
①稀硫酸溶液; ②浓盐酸; ③碳酸钠粉末;④Na2SO3溶液
写出图1烧瓶中发生反应的离子方程式为__________________________________________;
(2)甲同学所做实验图1烧杯中现象为____________________________________;
(3)乙同学所做实验图2中B处的现象为__________________________________;
(4)写出图2中A处发生反应的离子方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有5.1gNH3,则该气体的物质的量为__mol,该气体所含分子数为__个,该气体在标准状况下的体积为___L。实验室用密度为1.25g/mL,质量分数为36.5%浓盐酸配制250mL0.5mol/L的稀盐酸,浓盐酸的物质的量浓度为____,应量取浓盐酸的体积为____mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com