
【题目】按要求回答下列问题:
(1)键线式![]() 的系统命名为 __________________;
的系统命名为 __________________;
(2)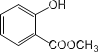 中含有的官能团名称为_______________;
中含有的官能团名称为_______________;
(3)2-甲基-1-丁烯的结构简式____________________;
(4) 的名称为________________;
的名称为________________;
(5)分子式为 C2H6O 的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是________________;
A.红外光谱 B.核磁共振氢谱 C.质谱法 D.与钠反应
【答案】2-甲基戊烷 羟基、酯基 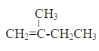 3-甲基-2, 5-己二醇 C
3-甲基-2, 5-己二醇 C
【解析】
(1)键线式![]() ,主链有5个碳原子,2号碳原子连有1个甲基,系统命名为2-甲基戊烷;
,主链有5个碳原子,2号碳原子连有1个甲基,系统命名为2-甲基戊烷;
(2) 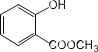 中含有的官能团为羟基、酯基;
中含有的官能团为羟基、酯基;
(3)根据系统命名原则,2-甲基-1-丁烯主链有4个碳,含一个双键在1号碳上,2号碳上有一个甲基,结构简式为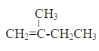 ;
;
(4) 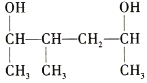 主链有6个碳,3号碳上有一个甲基,2、5号碳上有两个羟基,名称为:3-甲基-2, 5-己二醇;
主链有6个碳,3号碳上有一个甲基,2、5号碳上有两个羟基,名称为:3-甲基-2, 5-己二醇;
(5)乙醇(CH3CH2OH)、甲醚(CH3OCH3),官能团不同,能用红外光谱鉴别,不选A;
乙醇(CH3CH2OH)有3种等效氢、甲醚(CH3OCH3)有1种等效氢,能用核磁共振氢谱鉴别,不选B;
乙醇(CH3CH2OH)、甲醚(CH3OCH3)的相对分子质量相同,不能用质谱法鉴别,故选C;
乙醇(CH3CH2OH)与钠反应放出氢气、甲醚(CH3OCH3)与钠不反应,可以鉴别,不选D。
答案选C。


科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是
A.将Na2O2投入NH4Cl溶液中只可能生成一种气体
B.铁分别与稀盐酸和氯气反应,产物中铁元素的化合价相同
C.SO2通入BaCl2溶液有白色沉淀BaSO3生成
D.向滴有酚酞的Na2CO3溶液中加入足量CaCl2溶液,溶液红色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.1 g镁铝合金溶于60 mL 5.0mol·L![]() H
H![]() SO
SO![]() 溶液中,完全溶解后再加入a mL10.0 mol·L
溶液中,完全溶解后再加入a mL10.0 mol·L![]() 的NaOH溶液,此时溶液中的Mg
的NaOH溶液,此时溶液中的Mg![]() 、Al
、Al![]() 恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。
恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。
(1)当加入a=_________mLNaOH溶液时,可使溶液中的Mg![]() 和Al
和Al![]() 恰好完全沉淀。沉淀的最大值为__________ g。
恰好完全沉淀。沉淀的最大值为__________ g。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积___________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据测定结果绘制出ClO-、ClO3-等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是

A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.![]() 点溶液中存在如下关系:c(Na+)+ c(H+)=c(ClO-) +c(ClO3-) +c(OH-)
点溶液中存在如下关系:c(Na+)+ c(H+)=c(ClO-) +c(ClO3-) +c(OH-)
C.![]() 点溶液中各离子浓度:c(Na+)> c(Cl-) >c(ClO3-) =c(ClO-)> c(OH-) >c(H+)
点溶液中各离子浓度:c(Na+)> c(Cl-) >c(ClO3-) =c(ClO-)> c(OH-) >c(H+)
D.t2~t4,ClO-的物质的量下降的原因可能是ClO-自身歧化:2 ClO-=Cl-+ClO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是
A.用图 装置精炼铜,则a极为粗铜,电解质CuSO4溶液浓度变小
装置精炼铜,则a极为粗铜,电解质CuSO4溶液浓度变小
B.图 表示反应2SO2(g)+O2(g)
表示反应2SO2(g)+O2(g) ![]() 2SO3(g)增大O2的浓度对反应速率的影响
2SO3(g)增大O2的浓度对反应速率的影响
C.图 表示中和热测定的实验装置图
表示中和热测定的实验装置图
D.图 装置盐桥中KCl的Cl-移向左烧杯
装置盐桥中KCl的Cl-移向左烧杯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的常见化合价与原子序数的关系图:
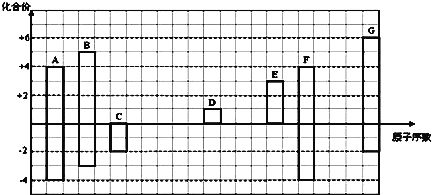
注:答题时,A—G所有元素都用其对应的元素符号表示。
(1)画出A的原子结构示意图______________;
(2)A的某氢化物分子式为A2H6,将含630mol电子的A2H6在氧气中完全燃烧生成稳定氧化物(H的稳定氧化物为液态)时放出的热量为QkJ,请写出表示1molA2H6完全燃烧的热化学方程式:_____________;
(3)用电子式表示D2G的形成过程______________;其所含化学键类型为________;
(4)C2-、D+、G2-离子半径大小顺序是___>____>____;
(5)C、G元素所形成的氢化物稳定性为___>____(填化学式),原因是:______________;
(6)某同学设计实验证明A、B、F的非金属性强弱关系, 装置如图。
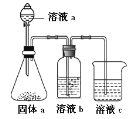
①溶液a和b分别为_________,__________;
②溶液c中发生反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。实验室利用下图装置制备亚硝酸钠,并测定所制亚硝酸钠的纯度。(加热装置及部分夹持装置已略去)
Ⅰ.亚硝酸钠的制备。
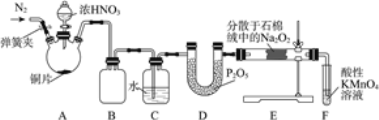
(1)盛放浓HNO3的仪器的名称为__________;装置B的作用是______________。
(2)装置E中制取NaNO2的化学方程式为___________________。
(3)多余的NO在装置F中被氧化为NO3-,反应的离子方程式为_____________。
(4)实验结束后打开A中弹簧夹,通入N2的目的是_______________。
Ⅱ.亚硝酸钠纯度的测定。
当Na2O2完全反应后,E中产生的固体除NaNO2外,还可能有NaNO3。测定亚硝酸钠纯度的步骤如下:
步骤一:取反应后的固体4.30 g溶于稀硫酸,向所得溶液中加入足量KI,将溶液中的NO2-和NO3-全部还原为NO,并通入足量N2,将NO全部赶出,最后将溶液稀释至1000 mL。
步骤二:取上述所得溶液10 mL,用淀粉作指示剂,用0.050 mol/L的Na2S2O3标准液滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,最终消耗Na2S2O3溶液体积为16.00 mL。
(5)步骤二中达到滴定终点的标志为______________________。
(6)混合固体中NaNO2的质量分数为________。(保留三位有效数字)
(7)若在滴定终点读取滴定管刻度时,仰视标准液液面,则测得亚硝酸钠的纯度________。(填“偏高”“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
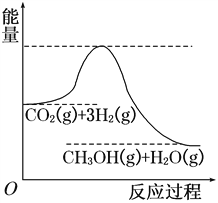
(1)上述反应平衡常数K的表达式为________________,温度降低,平衡常数K________(填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=________。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________(填写序号字母)。
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
Ⅱ、(1)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示(T1、T2均大于300℃)
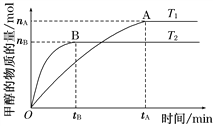
下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(2)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
①SO2、CS2、HI都是直线形的分子 ②价电子排布式为ns2的原子属于ⅠA或ⅡA族元素 ③Ge是ⅣA族的一种元素,其核外电子排布式为:[Ar]4s24p2,属于P区元素 ④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子⑤化合物NH4Cl和CuSO4·5H2O都存在配位键 ⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中 ⑦已知熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,则从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体 ⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为![]()
A.①③B.②④C.⑤⑥D.⑤⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com