
【题目】下列叙述正确的是
①SO2、CS2、HI都是直线形的分子 ②价电子排布式为ns2的原子属于ⅠA或ⅡA族元素 ③Ge是ⅣA族的一种元素,其核外电子排布式为:[Ar]4s24p2,属于P区元素 ④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子⑤化合物NH4Cl和CuSO4·5H2O都存在配位键 ⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中 ⑦已知熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,则从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体 ⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为![]()
A.①③B.②④C.⑤⑥D.⑤⑦⑧
【答案】C
【解析】
①CS2、HI都是直线形的分子,SO2是“V”形的分子,故①错误;②价电子排布式为ns2的原子属于ⅡA族元素或0族元素,故②错误;③Ge是ⅣA族的一种元素,其核外电子排布式为:[Ar]3d104s24p2,属于p区元素,故③错误;④非极性分子往往是高度对称的分子,比如BF3、PCl5、CO2这样的分子,H2O2是极性分子,故④错误;⑤化合物NH4Cl中铵根存在配位键,CuSO4·5H2O中[Cu(H2O)4]2+存在配位键,故⑤正确;⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中形成[Ag(NH3)2]+,故⑥正确;⑦HgCl2的稀溶液有弱的导电能力说明HgCl2是弱电解质,故⑦错误;⑧氨水中大部分NH3与H2O以氢键(用“···”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为![]() ,故⑧错误;因此⑤⑥正确,故C正确。
,故⑧错误;因此⑤⑥正确,故C正确。
综上所述,答案为C。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)键线式![]() 的系统命名为 __________________;
的系统命名为 __________________;
(2)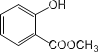 中含有的官能团名称为_______________;
中含有的官能团名称为_______________;
(3)2-甲基-1-丁烯的结构简式____________________;
(4) 的名称为________________;
的名称为________________;
(5)分子式为 C2H6O 的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是________________;
A.红外光谱 B.核磁共振氢谱 C.质谱法 D.与钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富马酸(反式丁烯二酸)与Fe2+形成的配合物——富马酸铁又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线:
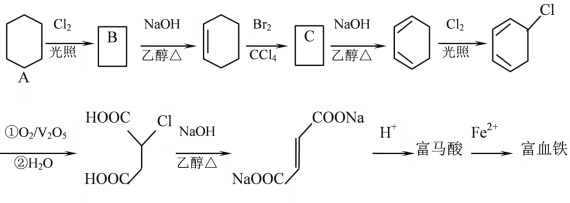
回答下列问题:
(1)A的化学名称为:_________________,由A生成B的反应类型为:___________
(2)C的结构简式为:______________,加热时,C与NaOH的乙醇溶液反应的化学方程式为:___________
(3)富马酸的结构简式为:___________
(4)检验富血铁中是否含有Fe3+的实验操作步骤是:___________
(5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应可放出_______L CO2(标况);富马酸的同分异构体中,同为二元羧酸的还有(写出结构简式):___________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于常见有机物的说法中正确的是( )
![]() 棉花、蚕丝和聚乙烯的主要成分都是纤维素
棉花、蚕丝和聚乙烯的主要成分都是纤维素
![]() 甲烷、乙醇和乙酸在一定条件下都能发生取代反应
甲烷、乙醇和乙酸在一定条件下都能发生取代反应
![]() 等质量的乙烷、乙烯、苯充分燃烧,消耗氧气的量由多到少
等质量的乙烷、乙烯、苯充分燃烧,消耗氧气的量由多到少
![]() 除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
![]() 苯分子中含有碳碳双键和单键,既能发生加成反应,也能发生取代反应
苯分子中含有碳碳双键和单键,既能发生加成反应,也能发生取代反应
![]() 石油分馏和煤的干馏属于物理变化,石油的裂化、裂解都属于化学变化
石油分馏和煤的干馏属于物理变化,石油的裂化、裂解都属于化学变化
A.①⑤⑥B.②③④C.①②③D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一般硫粉含有S(单斜)和S(正交)两种同素异形体。已知常温下:
①S(单斜)+O2(g) =SO2(g) ΔH=-297.16 kJ/mol
②S(正交)+O2(g) = SO2(g) ΔH=-296.83 kJ/mol
下列说法错误的是( )
A.S(g)+O2(g)=SO2(g) ΔH=-Q3 kJ/mol Q3> 297.16
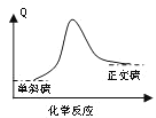
B.单斜硫转变为正交硫的能量变化可用如图表示
C.常温下单斜硫比正交硫稳定
D.单斜硫转化为正交硫的反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中加入4 mol A和2 mol B进行反应:3A(g)+2B(g) ![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后的压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后的压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=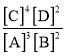 B.此时,B的平衡转化率是35%
B.此时,B的平衡转化率是35%
C.增大该体系的压强,平衡正向移动,化学平衡常数增大D.增加C,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用的几种气体发生装置如图A、B、C所示:
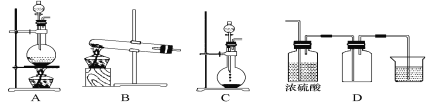
①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是___。
②气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是___(填序号,下同);
A.密度 B.颜色 C.溶解性 D.热稳定性 E.与氧气反应
③若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的___。
A.CO2 B.NO C.Cl2 D.H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知尿素的结构式为:![]() ,尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
,尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
(1)C、N、O三种元素的电负性由大到小顺序是__________。
(2) NH4+中H—N—H键角比NH3中H—N—H键角大,原因为______________________。
(3)美国科学家合成了结构呈“V”形的N5+,已知该离子中各原子均达到8电子稳定结构。则有关该离子的下列说法中正确的是_____。
A.每个N5+中含有35个质子和36个电子 B.该离子中有非极性键和配位键 C.该离子中含有2个π键 D.与PCl4+互为等电子体
(4)Fe(Ⅲ)除可与H2NCONH2形成配合物[Fe(H2NCONH2)6](NO3)3外,FeCl3溶液也可与KSCN溶液混合,得到含多种配合物的红色溶液,其中配位数为5的配合物的化学式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼泊金甲酯用作化妆品防腐剂,其结构为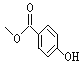 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.1mol尼泊金甲酯完全燃烧消耗7molO2
B.该化合物能与溴水反应,也能与NaHCO3反应
C.该化合物的同分异构体可能含有羧基
D.1mol该化合物最多可与4molH2反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com