
【题目】按要求填空:
(1)0.4mol OH﹣的质量为 , 其中含有个电子.
(2)质量比为16:7:6的三种气体S02、CO、NO,氧原子个数之比为;同条件下体积比为 .
(3)标准状况下,1体积水能溶解448体积HCl,所得溶液的密度为1.1g/mL,该溶液的质量分数和物质的量的浓度分别是、 . (保留1位小数)
【答案】
(1)6.8g,2.408×1024
(2)10:5:4,5:5:4
(3)42.2%,12.7mol?L﹣1
【解析】解:(1)OH﹣的摩尔质量为17g/mol,0.4mol OH﹣的质量为 0.4mol×17g/mol=6.8g,OH﹣含有10个电子,则0.4mol OH﹣含有电子数目为0.4mol×10×6.02×1023mol﹣1=2.408×1024,
故答案为:6.8g; 2.408×1024;
(2)质量比为16:7:6的SO2、CO、NO的物质的量之比为 ![]() :
: ![]() :
: ![]() =5:5:4,则含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下气体体积之比等于其物质的量之比,三者体积比为5:5:4,
=5:5:4,则含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下气体体积之比等于其物质的量之比,三者体积比为5:5:4,
故答案为:10:5:4;5:5:4;
(3)设水的体积为1L,则HCl的体积为448L,标况下HCl物质的量= ![]() =20molHCl质量为20mol×36.5g/mol=730g,溶液质量=1L×1000g/L+730g=1730g,
=20molHCl质量为20mol×36.5g/mol=730g,溶液质量=1L×1000g/L+730g=1730g,
溶液质量分数= ![]() ×100%=42.2%,
×100%=42.2%,
溶液体积= ![]() =
= ![]() L,则物质的量浓度为
L,则物质的量浓度为 ![]() =12.7molL﹣1.
=12.7molL﹣1.
故答案为:42.2%;12.7molL﹣1.
(1)利用![]() 求质量,
求质量,![]() 求微粒个数。(2)不同物质的
求微粒个数。(2)不同物质的![]() 之比即为其物质的量之比。(3)由水的体积可得水的质量,由HCl的体积可得HCl物质的量及其质量,水的质量与HCl的质量之和为溶液质量,再由溶液质量和其密度可得其体积,则HCl的质量与溶液质量可求得盐酸溶质质量分数、由HCl的物质的量与溶液体积可求得盐酸物质的量浓度。
之比即为其物质的量之比。(3)由水的体积可得水的质量,由HCl的体积可得HCl物质的量及其质量,水的质量与HCl的质量之和为溶液质量,再由溶液质量和其密度可得其体积,则HCl的质量与溶液质量可求得盐酸溶质质量分数、由HCl的物质的量与溶液体积可求得盐酸物质的量浓度。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知A,B,C,D之间的转化关系如图所示.下列说法正确的是( ) ![]()
A.若A为Fe,D为氢气,则B一定为酸
B.若A,D为化合物,B为水,则C一定是气体单质
C.若A,B,C,D均为化合物,该反应一定属于复分解反应
D.若A,B,C,D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s)△H=﹣444.3kJ/mol,在常温常压下能自发进行,对反应的方向起决定作用的是( )
A.焓变
B.温度
C.压强
D.熵变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mL Al2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1molL﹣1 Ba(OH)2溶液100mL,反应后溶液中SO42﹣的物质的量浓度约为( )
A.0.4 molL﹣1
B.0.3 molL﹣1
C.0.2 molL﹣1
D.0.1 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒容的密闭窗口中充入0.1mol/LCO2 , 0.1mol/L CH4 , 在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( ) 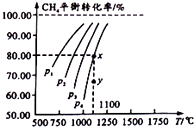
A.上述反应的△H<0
B.压强:P4>P3>P2>P1
C.1100℃时该反应平衡常数为1.64
D.压强为P4时,在y点:V正>V逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
A.27g Al3+所含离子数为3NA
B.11.2L氢气完全燃烧转移的电子数目为NA
C.常温常压下32g氧气所含的原子数目为2NA
D.标准状况下,22.4 L水中含有的水分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com