
【题目】对于反应4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s)△H=﹣444.3kJ/mol,在常温常压下能自发进行,对反应的方向起决定作用的是( )
A.焓变
B.温度
C.压强
D.熵变
科目:高中化学 来源: 题型:
【题目】含有其中离子的硫酸盐溶液:K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+、Cu2+ , 可以将它们一一鉴别出来的一种试剂是( )
A.KSCN
B.氨水
C.盐酸
D.NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( ) 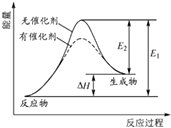
A.该反应为吸热反应
B.催化剂能改变反应的焓变
C.催化剂能降低反应的活化能
D.逆反应的活化能大于正反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数98%、密度为1.84g/cm3浓H2SO4来配制450mL、0.2mol/L的稀H2SO4 .
(1)经计算,需浓H2SO4的体积为 .
(2)除烧杯、玻璃棒、量筒外,配制上述溶液还需要的玻璃仪器是 .
(3)在配制过程中,其他操作都准确,下列操作中,能引起浓度偏高的有(填代号).
①将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4;
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中;
③洗涤溶解用的烧杯与玻璃棒,并将洗涤液转移到容量瓶中;
④转移前,容量瓶中含有少量蒸馏水;
⑤定容时,俯视标线;
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.3g钠投入到97.8g水中,反应完毕后,得到100mL的溶液.求:
(1)产生氢气在标况下的体积 .
(2)所得氢氧化钠溶液的溶质质量分数 .
(3)所得氢氧化钠溶液的物质的量浓度 .
(4)在K2Cr2O7+14HCl═2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为(标准状况),被氧化的HCl的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: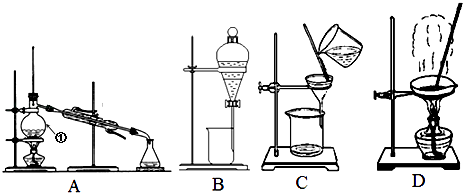
(1)从氯化钠溶液中得到氯化钠固体,选择装置(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置;从碘水中分离出I2 , 选择装置 , 该分离方法的名称为 .
(2)装置A中①的名称是 , 进冷却水的方向是 . 装置B在分液时为使液体顺利下滴,应进行的具体操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.4mol OH﹣的质量为 , 其中含有个电子.
(2)质量比为16:7:6的三种气体S02、CO、NO,氧原子个数之比为;同条件下体积比为 .
(3)标准状况下,1体积水能溶解448体积HCl,所得溶液的密度为1.1g/mL,该溶液的质量分数和物质的量的浓度分别是、 . (保留1位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.氢氧燃料电池在酸性介质中的正极反应式:O2+4H++4e﹣═2H2O
B.用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e﹣=Cu2+
D.反应HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0,在理论上能用于设计原电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com