
【题目】Na2CO3的制取方法及综合实验探究
(1)我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:

①往饱和食盐水中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是________________________。
②从生产流程图可知,可循环利用的物质是_____________。
③写出沉淀池中、煅烧炉中反应的化学方程式__________________。
(2)如何用CO2和50 mL 2 mol·L-1 NaOH溶液制取50 mL 1 mol·L-1 Na2CO3溶液?
①写出简要的实验步骤:_________________________________。
②写出有关反应的化学方程式:___________________________。
【答案】(1)①由于CO2在NaCl溶液中的溶解度很小,NH3在水中溶解度较大,先通入NH3使食盐水呈碱性,能够吸收大量CO2气体,产生较高浓度的HCO3-,才能析出NaHCO3晶体;②食盐水,CO2;③NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl、2NaHCO3Na2CO3+CO2↑+H2O↑;(2)①将50 mL 2 mol·L-1 NaOH溶液等分成两份,在一份NaOH溶液中通入过量的CO2气体,再将两溶液混合,即得50 mL 1 mol·L-1 Na2CO3溶液;②NaOH+CO2===NaHCO3、NaHCO3+NaOH===Na2CO3+H2O。
【解析】
试题分析:(1)①利用NaHCO3的溶解度小于Na2CO3,CO2虽然溶于水,但在水中溶解度小,NH3极易溶于水,先通入NH3使食盐水呈碱性,能够吸收大量CO2气体,产生较高浓度的HCO3-,才能析出NaHCO3晶体;②母液中通入氨气,母液中还有一部分是溶解的NaHCO3,因此产生NaCl,循环使用的是NaCl;③沉淀池中的反应是NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl,煅烧炉中发生的反应2NaHCO3![]() Na2CO3+CO2↑+H2O;(2)因为CO2与NaOH反应无色,通入CO2少量,NaOH过量,通入CO2过量产生NaHCO3,因此有将50 mL 2 mol·L-1 NaOH溶液等分成两份,在一份NaOH溶液中通入过量的CO2气体,加热,冷却后,再将两溶液混合,即得50 mL 1 mol·L-1 Na2CO3溶液;②NaOH+CO2===NaHCO3、NaHCO3+NaOH===Na2CO3+H2O。
Na2CO3+CO2↑+H2O;(2)因为CO2与NaOH反应无色,通入CO2少量,NaOH过量,通入CO2过量产生NaHCO3,因此有将50 mL 2 mol·L-1 NaOH溶液等分成两份,在一份NaOH溶液中通入过量的CO2气体,加热,冷却后,再将两溶液混合,即得50 mL 1 mol·L-1 Na2CO3溶液;②NaOH+CO2===NaHCO3、NaHCO3+NaOH===Na2CO3+H2O。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】【2016届雅安三诊】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的右图装置(夹持仪器未画出)进行定性实验。

请回答下列问题:
(1)假设2中的沉淀为 。
(2)假设1中沉淀为Cu(OH)2的理论依据是 。
(3)无水乙醇洗涤的目的____ __。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设______(填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用 试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是 。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:

(1)上述反应________(填“是”或“不是”)可逆反应。
(2)如图所示,表示NO2变化曲线的是 ________。用O2表示从0~2 s内该反应的平均速率v=________。
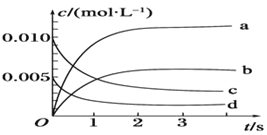
(3)能说明该反应已达到平衡状态的是_______(填序号)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Na2SO3溶液可与K2Cr2O7溶液反应,现有0.1mol//L的Na2SO3溶液12mL,恰好与0.04mol//L的K2Cr2O7溶液10mL完全反应,通过计算确定Cr元素在还原产物中的化合价
A.+1B.+3C.+4D.+5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学做如下实验,以检验反应中的能量变化。

实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是__________热反应;
(b)中温度降低, 根据能量守恒定律,(b)中反应物的总能量应该__________其生成物的总能量。
(2) 下列反应:①氢氧化钠与硫酸,②一氧化碳与氧气,③八水合氢氧化钡与氯化铵,④金属铜与硝酸银。其中(用序号填空): 能设计成原电池的反应是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )

A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类或归纳不正确的是( )
①电解质:明矾、冰醋酸、氯化银、纯碱
②化合物:BaCl2、Ca(OH)2、HNO3、HT
③混合物:盐酸、漂白粉、水玻璃、水银
④同素异形体:金刚石、石墨、C60
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:

(1)③⑤⑥⑦中原子半径最大的是 (用元素符号表示,下同),②③④⑤的简单离子中半径最小的是 。
(2)③⑤中元素的金属性强弱顺序为 ,⑥⑦元素的非金属性强弱顺序为 。
(3)①、②两种元素按原子个数比为1∶1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 。
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式 。
②写出电解A溶液的化学方程式: 。
③若上图中E、F按等物质的量进行反应,则混合物X中含有的物质有 (水忽略) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com