
【题目】下列离子方程式中正确的是( )
A. 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H2S↑
B. Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+=Fe2++2Fe3++4H2O
C. 碳酸氢铵溶液与过量的苛性钾溶液混和共热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D. 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→ (CH3)3COH+Cl-的能量与反应进程如图所示:

下列说法正确的是
A. 该反应为吸热反应
B. (CH3)3C+比(CH3)3 CCl稳定
C. 第一步反应一定比第二步反应快
D. 增大碱的浓度和升高温度均可加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列转化关系(反应条件略):

已知:①X、Y、Z、W均为氧化物.常态下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶液褪色.②相对分子质量:甲<乙.③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低.请填写下列空白:
(1)Z是(写化学式): .
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,反映出乙的浓溶液具有 性.利用这种性质可以进行 项(填字母)实验操作.
a.钝化铁片 b.检验Ba2+离子
c.干燥氨气 d.干燥氯气
(3)在X和Z的反应中,被氧化的X与被还原的X的物质的量之比是: .
(4)W可用于工业制溴过程中吸收潮湿空气中的Br2,写出该反应的化学方程式: .该反应很好地解决了环保问题,但给工业生产带来了 问题.
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.2gCu与足量的浓硫酸在加热条件下充分反应。
(1)请写出反应的方程式_________________;
(2)若把反应后的溶液稀释至500mL,取出50mL,向其中加入足量的BaCl2溶液,得到沉淀2.33g,则稀释后所得溶液中SO42-的物质的量浓度为_______________。
(3)若把反应后的溶液稀释至500mL,加入铁粉。最多能溶解__________g铁粉
(4)把产生的气体缓缓通入100mLamol/L的NaOH溶液中,若反应物均无剩余,则a的取值范围是___________________。
(5)若浓疏酸中含溶质bmol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的n(H2SO4)_______0.5bmol(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)根据氧化还原反应2H2+O2═2H2O,设计成燃料电池,负极通的气体应是 , 正极通的气体应是 .
(2)根据选择电解质溶液的不同,填写下表:
电解质溶液 | H2SO4溶液 | KOH溶液 |
负极反应式 |
|
|
正极反应式 |
|
|
溶液的pH变化 |
|
|
(3)若把H2改为CH4 , KOH作电解质,则负极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定量的稀HNO3中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。请将正确答案的序号填在相应的横线上。
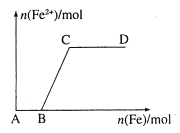
①Fe3+ ②Fe2+ ③Fe、Fe2+ ④Fe2+、Fe3+
(1)AB段铁元素以________形式存在。
(2)BC段铁元素以________形式存在。
(3)CD段铁元素以________形式存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某粒子的结构示意图为: 。请回答:
。请回答:
①当xy=10时,该粒子为________(填“原子”、“阳离子”或“阴离子”)。
②当y=8时,阳离子可能为(填离子符号)________、________。
(2)原子序数大于4的主族元素A和B的离子Am+和Bn它们的核外电子排布相同,据此推断:元素A和B所属周期序数之差为________;元素A和B的原子序数之差为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产、生活中有广泛应用,铜在化合物中的常见化合价有+1价、+2 价。已知Cu2O与稀硫酸反应,溶液呈蓝色。
(1)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为_______________。温度控制在50℃-60℃的两个原因除了加快反应速率外,还有____________________。在CuSO4溶液中加入一定量的Na2SO3和NaCl 溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式________________________________。
(2)现向Cu、Cu2O 和CuO组成的混合物中,加入1L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO 气体(标准状况)。Cu2O跟稀硝酸反应的离子方程式_______________________________。若将上述混合物用足量的H2加热还原,所得到固体的质量为___________g。若混合物中含0.1mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com