
����Ŀ��������ת����ϵ����Ӧ�����ԣ���

��֪����X��Y��Z��W��Ϊ�������̬�£�X�Ǻ���ɫ���壻Y��ʹ����ʯ��ˮ����ǵ�����ʹƷ����Һ��ɫ������Է����������ף��ң�������Ũ��Һ¶���ڿ�����һ��ʱ�䣬������СŨ�Ƚ��ͣ����ҵ�Ũ��Һ¶���ڿ�����һ��ʱ�䣬��������Ũ�Ƚ��ͣ�����д���пհף�
��1��Z�ǣ�д��ѧʽ���� ��
��2�����ҵ�Ũ��Һ¶���ڿ�����һ��ʱ�䣬��������Ũ�Ƚ��ͣ���ӳ���ҵ�Ũ��Һ���� �ԣ������������ʿ��Խ��� �����ĸ��ʵ�������
a���ۻ���Ƭ b������Ba2+����
c�����ﰱ�� d����������
��3����X��Z�ķ�Ӧ�У���������X�뱻��ԭ��X�����ʵ���֮���ǣ� ��
��4��W�����ڹ�ҵ������������ճ�ʪ�����е�Br2��д���÷�Ӧ�Ļ�ѧ����ʽ�� ���÷�Ӧ�ܺõؽ���˻������⣬������ҵ���������� ���⣮
��5��д��M���Ũ��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡���1��H2O����2����ˮ��d����3��2��1��
��4��SO2+Br2+2H2O=H2SO4+2HBr��ǿ����豸��ʴ��
��5��C+4HNO3��Ũ��![]() CO2��+4NO2��+2H2O��
CO2��+4NO2��+2H2O��
�����������������X��Y��Z��W��Ϊ�������̬�£�X�Ǻ���ɫ���壬��XΪNO2��Y��ʹ����ʯ��ˮ����ǵ�����ʹƷ����Һ��ɫ����YΪCO2������M��Ӧ�õ�����������������̼������֪��ΪHNO3��MΪ̼������̼��Ӧ�õ�������̼������������֪��ΪH2SO4����ZΪH2O��W�Ƕ�������
��1��������������֪��ZΪH2O��
��2��Ũ���������ˮ�ԣ�¶���ڿ�����һ��ʱ�䣬����������Ũ�Ƚ��ͣ��������ڸ����������������백����Ӧ�����ܸ��ﰱ����Ũ�������ǿ�����ԣ�����ʹFeƬ�ۻ����������������Ba2+���ӣ�
��3��X��Z�ķ�ӦΪ3NO2+H2O=2HNO3+NO���������Ķ�����������HNO3�������еĶ�����������NO���ɷ���ʽ��֪����������NO2�뱻��ԭ��NO2�����ʵ���֮����2��1��
��4�������ǿ�����ԣ�����Һ�н�������������Ϊ���ᣬ��������ԭΪHBr����Ӧ����ʽΪ��SO2+Br2+2H2O=H2SO4+2HBr����������ǿ�ᣬ�ڹ�ҵ����������ǿ����豸��ʴ���⣻
��5��̼��Ũ�����ڼ������������ɶ�����̼������������ˮ����Ӧ����ʽΪ��C + 4HNO3��Ũ��![]() CO2�� + 4NO2�� + 2H2O��
CO2�� + 4NO2�� + 2H2O��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���10mL0.1mol LCaCl2��Һ�еμ�0.1mol L ��Na2CO3��Һ���μӹ�������Һ��-lgc(Ca2+)��Na2CO3 ��Һ���(V)�Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ����

A. Z ���Ӧ�ķ�ɢϵ���ȶ�
B. w��x��y�����У�ˮ�ĵ���̶�����Ϊy��
C. ���õ�Ũ�ȵ�Na2SO4 ��Һ����Na2CO3 ��Һ����ͼ����x���ı仯�����߲�����ʾ
D. Ksp(CaCO3])=5 x 10-10mol2/L2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������仯��������������;�㷺��
I.����������ɰ�ķ���һһȷþ��(��Ҫ�ɷ�ΪMgCO3.SiO2������������Fe2O3��MnO��CaO��)Ϊ��Ҫԭ����ȡ����̼��þ[MgCO3:Mg(OH)2:2H2O]�Ĺ�ҵ��������:

��1��д��������"һ���У�MgCO3�����ᷴӦ�����ӷ���ʽ_____________��
��2������2����Ҫ�ɷ���MnO2��____��д������MnO2�����ӷ���ʽ__________��
��3�����ϳ���ʱ��ͨ������80�������ȱ߽��裬�¶Ȳ��ܳ�80����ԭ����______________��
II.�Ӻ�ͭ�ḻ����Ȼ��Դ��ͭ��(CuFeS2)ұ��ͭ�Ĺ�����������:

��֪:��CuFeS2+3CuCl2=4CuCl��+FeCl2+2S�� ��+1�۵�Cu���������������绯
��4����ȡʱ��������FeCl3��Һ��Ҳ������CuCl��S���÷�Ӧ��ѧ����ʽΪ________��
��5��������1������Һ��ֻ��FeCl2�������ڿ����м������ɡ����պ����ù���Ļ�ѧʽΪ______��
��6��������Һ��pH������Cu�⣬���ܲ���һ�ֽ������ӣ��˽���������______���������ӷ��ţ�
��7������3������Һ�е�CuCl2��ѭ��ʹ�ã�Ϊ�������̳���ѭ����ÿ����1molCu���������貹��CuCl2�����ʵ���Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H+��Na+��Ba2+��Fe3+��Al3+��SO42����CO32- �����ӡ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ����ͼ��ʾ�������ж���ȷ����

A. ԭ��Һ��һ������H+��Fe3+��Al3+�����ܺ�Ba2+
B. ԭ��Һ�к�Fe3+��Al3+�����ʵ���֮��Ϊl��l
C. ԭ��Һ�п��ܺ���CO32-
D. ��Ӧ����γɵ���Һ�к��е�����ֻ��NaAlO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij���������Ļ����Һ20mL�����к��������Ũ��Ϊ2mol��L-1���������Ũ��Ϊ
1mol��L-1���������м���0.96gͭ�ۣ���ַ�Ӧ����ֻ����NO���壩�������ռ���
��״���µ���������Ϊ
A. 89.6mL B. 112mL
C. 168mL D. 224mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС���ͬѧ������ͼ����֤ijͭ���Ͻ���ȫ�ܽ���Ũ��������ɵ������NO2�����NO�����ⶨ�Ͻ���ͭ��������������֪������NO2��N2O4��ϴ��ڣ��ڵ���0��ʱ����ֻ����ɫ��N2O4���塣

(1)д��A��ͭ�����ᷴӦ��һ����ѧ����ʽ________________________��
(2)��Ӧǰ�ȴ�A���ֵĻ���K������ͨ��һ��ʱ���N2��������_______________����װ����ȱ��B���֣���Ӱ����֤�Ľ������ԭ����____________________��
(3)��Ӧ��������K2����ͨ��O2������NO��������D������������_________��
(4)ʵ���õ��������£��Ͻ�����15.0g��13.5mol/LHNO340mL��ʵ���A��Һ��V=40 mL��c(H+)=1.0mol/L�����跴Ӧ�������ӷ�Ҳû�зֽ⡣��Ӧ�����ĵ�HNO3���ʵ���Ϊ____________mol��
(5)����Aװ���з�Ӧ����ҺҲ��ȷ��ͭ������������������ȡ��A�еķ�Ӧ����Һ�������м���������_____��Һ��Ȼ����еIJ����IJ���ֱ���____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����ȷ����( )
A. ������ͭ��Һ�м��������NaHS��Һ��Cu2++2HS-=CuS��+H2S��
B. Fe3O4�ܽ��ڹ�����ϡ�����У�Fe3O4+8H+=Fe2++2Fe3++4H2O
C. ̼�������Һ������Ŀ��Լ���Һ����ȣ�NH4++OH-![]() NH3��+H2O
NH3��+H2O
D. ������SO2����ͨ��NaClO��Һ�У�SO2+2ClO-+H2O=SO32-+2HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�Ƿ�������ʱ���õ��������������ң����Խ��еĻ�����������ֱ��ǣ� �� 
A.������������ȡ������
B.�����ˡ���ȡ������
C.��ȡ�����ˡ���������
D.���ˡ���������ȡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������Mg-Al�Ͻ�Ͷ��100mLһ�����ʵ���Ũ�ȵ�ijHCl��Һ�У���ַ�Ӧ����Ӧ�����Һ����μ���һ�����ʵ���Ũ�ȵ�NaOH��Һ�����ɳ���������������NaOH��Һ�������ϵ����ͼ���ش��������⣺
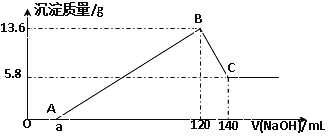
��1��д��OA�κ�BC�η�Ӧ�����ӷ���ʽ��
OA��________________________________ �� BC��_____________________________��
��2��ԭMg-Al�Ͻ��������_____________��
��3��ԭHCl��Һ�����ʵ���Ũ����________________��
��4������NaOH��Һ�����ʵ���Ũ����____________��
��5��a��ֵ��____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com