
【题目】乙烯是重要的有机合成基础原料。以下是由乙烯合成高分子化合物PVB、缩醛M、碳酸二甲酯等重要有机物的合成路线。
 已知:醛与二元醇可生成环状缩醛:
已知:醛与二元醇可生成环状缩醛:![]()
请回答下列问题:
(1)B的名称是______________, C的名称是__________。
(2)反应③的反应类型是_____________,缩醛M的分子式是_____________。
(3)反应④的化学方程式是___________。
(4)D的结构简式是 ___________。
(5)缩醛M有多种同分异构体,其中属于羧酸,且苯环上只有两个取代基的同分异构体共有_______种。
(6)参照的合成路线,设计一条由2-溴丙烷制备 的合成路线(注明必要的反应条件):
的合成路线(注明必要的反应条件):
_________________________________________。
【答案】 苯乙醛 乙二醇 取代反应 C10H12O2 CH3CH2CH2CHO ![]() 15
15 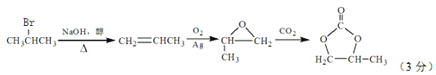
【解析】试题分析:根据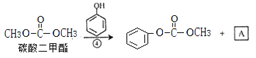 ,可知A是甲醇;
,可知A是甲醇;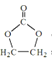 与甲醇反应生成C和碳酸二甲酯,所以C是HOCH2CH2OH;乙二醇与B反应生成
与甲醇反应生成C和碳酸二甲酯,所以C是HOCH2CH2OH;乙二醇与B反应生成![]() ,B的结构是
,B的结构是![]() ;
; ,D是丁醛;
,D是丁醛;
解析:(1)![]() 的名称是苯乙醛, HOCH2CH2OH的名称是乙二醇。
的名称是苯乙醛, HOCH2CH2OH的名称是乙二醇。
(2) 与甲醇反应生成乙二醇和碳酸二甲酯的反应类型是取代反应,根据结构简式
与甲醇反应生成乙二醇和碳酸二甲酯的反应类型是取代反应,根据结构简式![]() 的分子式是C10H12O2;
的分子式是C10H12O2;
(3)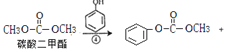 甲醇
甲醇
的化学方程式是![]() 。
。
(4)D是丁醛,结构简式是CH3CH2CH2CHO。
(5)缩醛M有多种同分异构体,其中属于羧酸,且苯环上只有两个取代基的同分异构有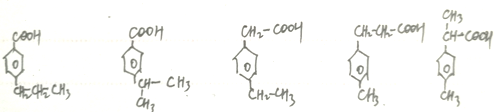 各有邻、间、对3种,共15种。
各有邻、间、对3种,共15种。
(6)根据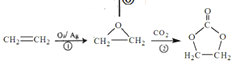 ,
,
由2-溴丙烷制备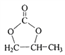 ,先由2-溴丙烷消去,制取丙烯,再氧化为甲基环氧乙烷,合成路线为
,先由2-溴丙烷消去,制取丙烯,再氧化为甲基环氧乙烷,合成路线为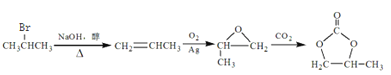 。
。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】1,6﹣己二胺(H2N﹣(CH2)6﹣NH2)毒性较大,可引起神经系统、血管张力和造血功能的改变.下列化合物中能与它发生化学反应的是( )
A. NaOHB. Na2CO3C. NaClD. HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol 配合物与足量AgNO3溶液作用生成1 mol AgCl沉淀,则m、n的值是
A.m=1,n=5 B.m=3,n=4
C.m=5,n=1 D.m=3,n=3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. Fe(SCN)3溶液中存在Fe3++3SCN-![]() Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深
Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深
B. 用通过盛饱和食盐水的洗气瓶来除去氯气中的少量HCl气体杂质
C. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)(正反应为放热反应)。达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应)。达平衡后,升高温度体系颜色变深
D. 合成氨:N2(g)+3H2(g)![]() 2NH3(g) △H<0在高温、高压和催化剂条件下进行
2NH3(g) △H<0在高温、高压和催化剂条件下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】〔化学——选修3:物质结构与性质〕举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步。探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术。已知所用火箭推进剂为肼(N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为 ,第一电离能最大的元素为 。
(2)钛的原子序数为22,其基态电子排布式示意图为 。
(3)1 mol N2H4分子中含有的键数目为 。
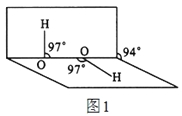
(4)H2O2分子结构如图1,其中心原子杂化轨道为 ,估计它难溶于CS2,简要说明原因 。
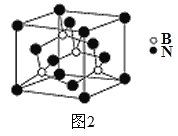
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为 ,若立方氮化硼的密度为g·cm-3,阿伏加德罗常数为NA,则两个最近N原子间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或事故处理正确的是
A. 金属钠着火,立即用水扑灭
B. 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中
C. 实验结束后,用嘴吹灭酒精灯
D. 皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
① C2H2(g) +5/2O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJmol-1
③ H2(g)+ ![]() O2(g) == H2O(1) △H3 = -285.8 kJ·mol-1
O2(g) == H2O(1) △H3 = -285.8 kJ·mol-1
则反应④ 2C(s)+ H2(g) == C2H2(g)的△H为( )
A. +228.2 kJ·mol-1 B. -228.2 kJ·mol-1
C. +1301.0 kJ·mol-1 D. +621.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜的配合物A结构如图图1。请回答下列问题:

(1)写出基态Cu的外围电子排布式________
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和x键数目之比是___;N2O与CO2互为等电子体,则N2O的电子式为_______。
(3)在Cu催化下,甲醇可被氧化为甲醛,甲醇分子中HCO的键角____(选填“大于”、“等于”或“小于”) l20°;甲醛能与水形成氢健,请在如图2中表示出来____。


(4)立方氮化硼如图3、图4与金刚石结构相似,是超硬材料。立方氮化硼晶体内B一N键数与硼原子数之比为__________;
(5)Cu晶体的堆积方式如图5所示,设Cu原子半径为a,晶体中Cu原子的配位数为_____,晶体的空间利用率为_________。(已知:![]() ,列式并计算出结果)
,列式并计算出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com